题目内容
【题目】已知H2O2在催化剂作用下分解速率加快,其能量随反应进程的变化如图所示,下列说法正确的是( )

A. 加入催化剂,减小了反应的热效应
B. 该反应的热化学方程式:2H2O2(l)===2H2O(l)+O2(g) ΔH>0
C. 双氧水催化分解不需要加热,由此推测,催化剂存在下的分解都不需要加热
D. 该反应的反应物总能量高于生成物总能量
【答案】D
【解析】A.催化剂只通过改变活化能来改变反应速率,不改变反应的热效应;故A错误;B.图象分析判断反应是放热反应,热化学方程式要注明状态,所以H2O2分解的热化学方程式:H2O2(l)=H2O(l)+![]() O2(g)△H>0,故B错误;C.催化剂只改变反应速率不改变反应的热效应,有的反应使用催化剂后反应仍需要加热,如氯酸钾和二氧化锰混合加热制氧气,故C错误;D.图象分析反应是放热反应,所以反应物的总能量高于生成物的总能量,故D正确;故选D。
O2(g)△H>0,故B错误;C.催化剂只改变反应速率不改变反应的热效应,有的反应使用催化剂后反应仍需要加热,如氯酸钾和二氧化锰混合加热制氧气,故C错误;D.图象分析反应是放热反应,所以反应物的总能量高于生成物的总能量,故D正确;故选D。

 亮点激活精编提优100分大试卷系列答案
亮点激活精编提优100分大试卷系列答案【题目】某小组同学做“硫在氧气中燃烧”的实验时,老师建议在集气瓶底部放少量NaOH溶液吸收生成的SO2。这种做法引起了同学们的思考:SO2与NaOH是否发生反应。
【查阅资料】通常状况下,1体积水约能溶解40体积SO2。
【实验方案】同学们向充满SO2的软塑料瓶中迅速倒入一定量NaOH溶液,拧紧瓶盖,振荡,发现塑
料瓶变瘪,他们认为SO2与NaOH发生了反应。
【反思与改进】甲同学认为上述实验不够严谨,理由是_________________。于是同学们设计了如下两
个改进方案。
方案一:
实验操作 | 实验现象 |
向两个充满SO2的200 mL软塑料瓶中分别注入10 mL水和NaOH溶液,振荡,对比。 | 两个瓶子变瘪的程度完全相同 |
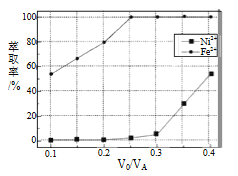
乙同学认为由于两个瓶子变瘪的程度完全相同,因此无法证明SO2与NaOH是否发生了反应。试分析导致两个瓶子变瘪的程度完全相同的原因是_____________________。他认为若改变注入水和NaOH溶液的体积便可达到实验目的,注入液体的体积可以是__________(填序号)。
a.15 mL b.8 mL c.5 mL d.3 mL
方案二:
实验操作 | 实验现象 |
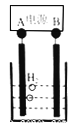
利用如图所示装置进行实验: 向两个充满SO2的300 mL集气瓶 中分别加入6 mL水和NaOH溶液, 一段时间后,打开止水夹,对比。
| 倒吸入两个集气瓶中的液体体积完全相同 |
丙同学认为上述方案也无法证明SO2与NaOH是否发生反应。你认为导致吸入液体的体积完全相同的原因是___________________。
丁同学思考后,将上述装置进行了改进,便达到实验目的。改进装置如下图所示,你认为装置B的作用是_______________。