题目内容
13.下列说法正确的是( )| A. | 氯水要现用现制,并保存在盖有橡胶塞的棕色瓶子中,置于冷暗处 | |
| B. | Na2O的水溶液能导电,不能说明Na2O是电解质 | |
| C. | 石英和玛瑙的主要成分均为二氧化硅,其分子式为SiO2 | |
| D. | 酸性氧化物大多数是非金属氧化物,因此一定不能与酸溶液发生反应 |
分析 A.氯水在含HClO光照分解,且氯水能氧化橡胶;
B.Na2O与水反应生成电解质;
C.二氧化硅为原子晶体,不存在分子;
D.二氧化硫为酸性氧化物,能够与硝酸发生氧化还原反应.
解答 解:A.氯水在含HClO光照分解,且氯水能氧化橡胶,则氯水要现用现制,并保存在盖有玻璃塞的棕色瓶子中,置于冷暗处,不能使用橡皮塞,故A错误;
B.Na2O与水反应生成电解质NaOH,所以Na2O的水溶液能导电,这不能说明Na2O是电解质,故B正确;
C.二氧化硅为原子晶体,不存在分子,没有分子式,故C错误;
D.二氧化硫为酸性氧化物,能够与硝酸发生氧化还原反应,故D错误;
故选B.
点评 本题考查了元素化合物知识,明确电解质、酸性氧化物的概念,注意只有分子晶体才存在分子式,题目难度不大.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
3. 在2L密闭容器内,800℃时反应:2NO(g)+O2(g)?2NO2(g)体系中,n(NO)随时间的变化如下表:
在2L密闭容器内,800℃时反应:2NO(g)+O2(g)?2NO2(g)体系中,n(NO)随时间的变化如下表:
(1)上述反应是(填“是”或“不是”)可逆反应,在第5s时,NO的转化率为65%.
(2)如图中表示NO2的变化的曲线是b,用O2表示从0~2s内该反应的平均速率v=1.5×10-3mol•L-1•s-1.
 在2L密闭容器内,800℃时反应:2NO(g)+O2(g)?2NO2(g)体系中,n(NO)随时间的变化如下表:
在2L密闭容器内,800℃时反应:2NO(g)+O2(g)?2NO2(g)体系中,n(NO)随时间的变化如下表:| 时间(s) | 0 | 1 | 2 | 3 | 4 | 5 |
| N(NO)(mol) | 0.020 | 0.01 | 0.008 | 0.007 | 0.007 | 0.007 |
(2)如图中表示NO2的变化的曲线是b,用O2表示从0~2s内该反应的平均速率v=1.5×10-3mol•L-1•s-1.
4.下列说法正确的是( )
| A. | 甲烷的标准燃烧热为-890.3 kJ•mol-1,则甲烷燃烧的热化学方程式表示为:CH4(g)+2O2(g)=CO2(g)+2H2O(g)△H=-890.3 kJ•mol-1 | |
| B. | 500℃、30 Mpa下,将0.5 mol N2和1.5 mol H2置于密闭的容器中充分反应生成NH3(g),放热19.3kJ,其热化学方程式为:N2(g)+3H2(g)?2NH3(g)△H=-38.6kJ•mol-1 | |
| C. | 同温同压下,H2(g)+Cl2(g)=2HCl(g)在光照和点燃条件的△H相同 | |
| D. | HCl和NaOH反应的中和热△H=-57.3kJ/mol,则H2SO4和Ca(OH)2反应的中和热△H=2×(-57.3)kJ/mol |
1.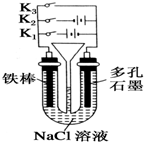 按如图所示装置进行下列不同的操作,其中不正确的是( )
按如图所示装置进行下列不同的操作,其中不正确的是( )
 按如图所示装置进行下列不同的操作,其中不正确的是( )
按如图所示装置进行下列不同的操作,其中不正确的是( )| A. | 铁腐蚀的速度由大到小的顺序是:只接通K1>只闭合K3>都断开>只闭合K2 | |
| B. | 只接通K1,一段时间后,U形管中出现白色沉淀 | |
| C. | 只接通K2,U形管左、右两端液面均下降 | |
| D. | 先只接通K1,一段时间后,漏斗液面上升,然后再只接通K2,漏斗液面下降 |
18.下列说法中正确的是( )
| A. | 0.1mol•L-1的NaCl溶液中,Na+与Cl-离子总数为0.2NA | |
| B. | 标准状况下,2.24L水的质量是1.8g | |
| C. | 16gO3比16gO2所含的氧原子数多 | |
| D. | 22gCO2与标准状况下11.2L Cl2含有相同的分子数 |
5.进行化学实验时应强化安全意识.下列做法正确的是( )
| A. | 酒精灯被打翻并着火时可用水扑火 | |
| B. | 浓硫酸溅到皮肤上时立即用大量水冲洗 | |
| C. | 用试管加热高锰酸钾固体制氧气时使试管口倾斜向上 | |
| D. | 为避免浪费,用剩的药品一般应放回原试剂瓶 |
2.据预测,月球的土壤中吸附着数百万吨的氦${\;}_{2}^{3}$He,可作为未来核聚变的重要原料之一.对${\;}_{2}^{3}$He原子的叙述不正确的是( )
| A. | 质量数是3 | B. | 质子数是3 | C. | 中子数是1 | D. | 电子数是2 |
3.下列属于加成反应的是( )
| A. | CH4+Cl2$\frac{\underline{\;光照\;}}{\;}$CH3Cl+HCl | |
| B. | CH3COOH+CH3CH2OH→CH3COOC2H5+H2O | |
| C. |  | |
| D. | CH2=CH2+Br2→BrCH2CH2Br |