题目内容
16.用NA代表阿伏加德罗常数的值,下列说法正确的是( )| A. | 100mL lmol/L的FeCl3溶液完全生成Fe(OH)3胶体,其胶粒数目为0.1NA | |
| B. | 7.8 g Na2O2中含有的离子总数目为0.4NA | |
| C. | 30g SiO2晶体中含有Si-O键的数目为2NA | |
| D. | 标准状况下44.8L HF溶于水配成溶液中所含F-的数目为2NA |
分析 A.胶体微粒是氢氧化铁的集合体;
B.过氧化钠是由钠离子和过氧根离子构成;
C.二氧化硅中含有4个Si-O键;
D.氟化氢为弱电解质,水溶液中部分电离.
解答 解:A.100mL lmol/L的FeCl3溶液完全生成Fe(OH)3胶体,其胶粒数目远远小于0.1NA,故A错误;
B.7.8 g Na2O2的物质的量为7.8g78g/mol7.8g78g/mol=0.1mol,含有0.2mol钠离子和0.1mol过氧根离子,共含有的离子总数目为0.3NA,故B错误;
C.30g SiO2晶体的物质的量为30g60g/mol30g60g/mol=0.5mol,二氧化硅中含有4个Si-O键计算判断,30g SiO2晶体中含有Si-O键的数目为2NA,故C正确;
D.氟化氢为弱电解质,水溶液中部分电离,所以标准状况下44.8L HF溶于水配成溶液中所含F-的数目小于2NA,故D错误;
故选:C.
点评 本题考查了阿伏伽德罗常数的分析应用,主要是胶体微粒组成,物质结构分析判断,掌握基础是关键,注意弱电解质电离特点,题目难度不大.

练习册系列答案
相关题目
7.碳酸铜和碱式碳酸铜〔Cu2(OH)2CO3〕均可溶于盐酸,转化为氯化铜.在高温下这两种化合物均能分解生成氧化铜.溶解28.4g的上述混合物,消耗2mol•L-1的盐酸250mL.灼烧等量的上述混合物,得到氧化铜的质量是( )
| A. | 40 g | B. | 30 g | C. | 20 g | D. | 15 g |
11.下列石油制品中,沸点范围最低的是( )
| A. | 柴油 | B. | 润滑油 | C. | 汽油 | D. | 煤油 |
8.向氯酸钠的酸性水溶液中通入二氧化硫,反应中氧化过程为:SO2+2H2O-2e-→SO42-+4H+;向亚氯酸钠(NaClO2)固体中通入用空气稀释的氯气,反应中还原过程为:Cl2+2e-→2Cl-.在上述两个反应中均会生成产物X,则X可能是( )
| A. | ClO2 | B. | NaClO4 | C. | HClO | D. | NaClO |
6.60276027Co是γ放射源,60276027Co可用于农作物的诱变育种,我国用该方法培育出了许多农作物新品种.对原子60276027Co的叙述不正确的是( )
| A. | 质量数是60 | B. | 质子数是27 | C. | 中子数是33 | D. | 电子数是33 |
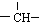 和一个-Cl,它的可能结构有四种,请写出它们的结构简式:CH3CH2CH2CHClCH3、CH3CH2CHClCH2CH3、CH3CH(CH3)CH2CH2Cl、CH2ClCH(CH3)CH2CH3.
和一个-Cl,它的可能结构有四种,请写出它们的结构简式:CH3CH2CH2CHClCH3、CH3CH2CHClCH2CH3、CH3CH(CH3)CH2CH2Cl、CH2ClCH(CH3)CH2CH3.