题目内容
向一容积为1L的密闭容器中加入一定量的X、Y,发生化学反应aX(g)+2Y(s)  bZ(g);△H<0。右图是容器中X、Z的物质的量浓度随时间变化的曲线。
bZ(g);△H<0。右图是容器中X、Z的物质的量浓度随时间变化的曲线。

根据以上信息,下列说法正确的是
 bZ(g);△H<0。右图是容器中X、Z的物质的量浓度随时间变化的曲线。
bZ(g);△H<0。右图是容器中X、Z的物质的量浓度随时间变化的曲线。
根据以上信息,下列说法正确的是
| A.用X表示0~10min内该反应的平均速率为v(X)=0.045mol/L·min |
| B.根据上图可求得方程式中a:b= 1:3, |
| C.推测在第7min时曲线变化的原因可能是升温 |
| D.推测在第13min时曲线变化的原因可能是降温 |
C
试题分析:0~10min内该反应的平均速率为v(X)=
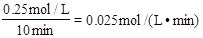 ,A项错误;0~10min内X的变化量是0.25mol/L,Z的变化量是0.5mol/L,所以a:b=1:2,B项错误;7min时从图中可以看出速率加快,但浓度没有改变,所以不是增大压强和增加浓度,有可能是升高温度,C项正确;13min时从图中可以看出X浓度增加,Z的浓度减小,说明平衡逆向移动,不可能是降温,D项错误。答案选C。
,A项错误;0~10min内X的变化量是0.25mol/L,Z的变化量是0.5mol/L,所以a:b=1:2,B项错误;7min时从图中可以看出速率加快,但浓度没有改变,所以不是增大压强和增加浓度,有可能是升高温度,C项正确;13min时从图中可以看出X浓度增加,Z的浓度减小,说明平衡逆向移动,不可能是降温,D项错误。答案选C。点评:在分析有关图像时应该注意:一、ν-t 图像或 c-t 图像:1.ν-t 图像:分清正逆反应,分清各因素(浓度、温度、压强、催化剂)对反应速率和平衡移动的影响。 二、平衡图像 1.出现拐点的图像:分析依据“先拐先平”。在转化率-时间图像或物质的百分含量-时间图像中,先出现拐点的曲线先达到平衡(代表温度高或压强大或使用合适的催化剂等)。

练习册系列答案
相关题目
 2HI(g);△H<0,并达平衡。HI的体积分数w(HI)随时间变化如图曲线(Ⅱ)所示
2HI(g);△H<0,并达平衡。HI的体积分数w(HI)随时间变化如图曲线(Ⅱ)所示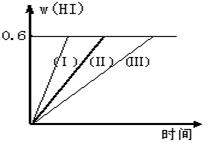
 2NH3(g) ;△H=" —92.4" KJ·mol—1。现在500℃、20 MPa时,将N2、H2置于一个容积为2 L的密闭容器中发生反应,反应过程中各物质的物质的量变化如下图。回答下列问题:
2NH3(g) ;△H=" —92.4" KJ·mol—1。现在500℃、20 MPa时,将N2、H2置于一个容积为2 L的密闭容器中发生反应,反应过程中各物质的物质的量变化如下图。回答下列问题: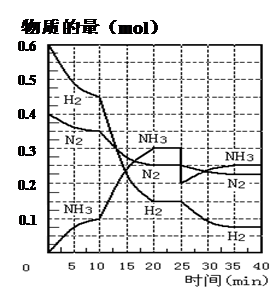
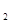 (g)+1/2O
(g)+1/2O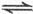 SO
SO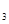 (g)△H=-98.32kJ/mol,现有4molSO
(g)△H=-98.32kJ/mol,现有4molSO CO2(g) +H2 (g),向2 L密闭容器中通入2 mol CO (g)、1 mol H2O (g),2 min后反应达到平衡时,测得CO的物质的量为1.6mol,用H2O (g)表示该反应速率为________此温度下,该反应的平衡常数为________若往容器中再加入2 mol CO (g),则重新达到平衡时的CO总转化率________20%(填“>”、“<”或“=”)。
CO2(g) +H2 (g),向2 L密闭容器中通入2 mol CO (g)、1 mol H2O (g),2 min后反应达到平衡时,测得CO的物质的量为1.6mol,用H2O (g)表示该反应速率为________此温度下,该反应的平衡常数为________若往容器中再加入2 mol CO (g),则重新达到平衡时的CO总转化率________20%(填“>”、“<”或“=”)。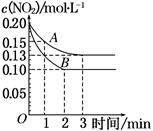
 2Z(g)。此反应达到平衡的标志是 ( )
2Z(g)。此反应达到平衡的标志是 ( ) 2CH3OH(g)在恒容密闭容器中进行。为探究温度、CO2等因素对该反应的影响,进行了4组实验,结果如右下表。下列说法不正确的是
2CH3OH(g)在恒容密闭容器中进行。为探究温度、CO2等因素对该反应的影响,进行了4组实验,结果如右下表。下列说法不正确的是