题目内容
9.下表为元素周期表的一部分,请参照元素①-⑧在表中的位置,用元素符号或化学用语回答下列问题:
(1)①和②形成的最简单有机化合物分子的结构式为
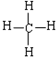 .
.(2)下列事实能证明②的非金属性比⑥强的是CD.
A.Na2CO3+SiO2$\frac{\underline{\;高温\;}}{\;}$Na2SiO3+CO2↑
B.SiO2+2C$\frac{\underline{\;高温\;}}{\;}$Si+2CO↑
C.Na2SiO3+CO2+2H2OH2SiO3↓+Na2CO3
D.CH4比SiH4稳定
(3)写出①、③、④三种元素组成化合物的电子式
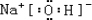 .
.(4)③、④、⑤的形成的简单离子半径依次减小(填“增大”、“减小”或“不变”).
(5)①、②、⑦三种元素按原子个数之比为11:5:1组成的有机化合物中含有两个-CH3的同分异构体有4种.
分析 由元素在周期表中的位置可知,①是H元素、②为C元素、③是O元素、④是Na、⑤是Al元素、⑥是Si元素、⑦为Cl元素,
(1)①和②形成的最简单有机化合物为甲烷,甲烷分子中含有4个碳氢键,为正四面体结构;
(2)A.该反应为高温固体之间的反应,不能判断非金属性强弱;
B.该反应中C的还原性大于Si的还原性,无法比较C、Si的非金属性;
C.非金属性越强,最高价氧化物对应的水化物的酸性越强,该反应为强酸制取弱酸的反应,可以判断非金属性强弱;
D.CH4比SiH4稳定,可知C的非金属性强;
(3)①、③、④三种元素组成化合物为NaOH,氢氧化钠为离子化合物,阴阳离子需要标出所带电荷;
(4)电子层越多,离子半径越大,电子层相同时核电荷数越大,离子半径越小;
(5)三种元素按原子个数之比为11:5:1组成的有机化合物为C5H11Cl,根据同分异构体的书写原则写出满足条件的有机物的结构简式.
解答 解:由元素在周期表中的位置可知,①是H元素、②为C元素、③是O元素、④是Na、⑤是Al元素、⑥是Si元素、⑦为Cl元素,
(1)①和②形成的最简单有机化合物为甲烷,甲烷为正四面体结构,甲烷的结构式为: ,
,
故答案为: ;
;
(2)A.Na2CO3+SiO2$\frac{\underline{\;高温\;}}{\;}$Na2SiO3+CO2↑,为高温固体之间的反应,不能比较非金属性,故A错误;
B.SiO2+2C$\frac{\underline{\;\;△\;\;}}{\;}$Si+2CO↑中,C的还原性大于Si的还原性,不能比较C、Si的非金属性,故B错误;
C.Na2SiO3+CO2+2H2O═H2SiO3↓+Na2CO3,发生强酸制取弱酸的反应,可知C的非金属性强,故C正确;
D.非金属性越强,温度下越强,根据CH4比SiH4稳定可知C的非金属性强,故D正确;
故答案为:CD;
(3)①、③、④三种元素组成化合物为NaOH,其电子式为: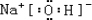 ,
,
故答案为: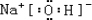 ;
;
(4)③、④、⑤的离子具有相同电子结构,原子序数大的离子半径小,则③、④、⑤的形式的简单离子半径依次减小,
故答案为:减小;
(5)①、②、⑦三种元素按原子个数之比为11:5:1组成的有机化合物为C5H11Cl,分子式为C5H11Cl的同分异构体有
主链有5个碳原子的:CH3CH2CH2CH2CH2Cl、CH3CH2CH2CHClCH3、CH3CH2CHClCH2CH3;
主链有4个碳原子的:CH3CH(CH3)CH2CH2Cl、CH3CH(CH3)CHClCH3、CH3CCl(CH3)CH2CH3、CH2ClCH(CH3)CH2CH3;
主链有3个碳原子的:CH3C(CH3)2CH2Cl;
含有两个-CH3的同分异构体有CH3CH2CH2CHClCH3、CH3CH2CHClCH2CH3、CH3CH(CH3)CH2CH2Cl、CH2ClCH(CH3)CH2CH3,共4种,
故答案为:4.
点评 本题考查元素周期表和元素周期律的综合应用,为高频考点,题目难度中等,注意明确有机物的结构及同分异构体,熟练掌握元素周期表结构、元素周期律内容,试题培养了学生的分析、理解能力及灵活应用能力.

 备战中考寒假系列答案
备战中考寒假系列答案| A. | O2、O3 | B. | Na2O、Na2O2 | C. | 40K、40Ca | D. | H、D、T |
 化学平衡mA(g)+nB(g)?pC(g)+qD(g),如图所示是A的转化率同压强,温度的关系,分析图象可以得出的正确结论是( )
化学平衡mA(g)+nB(g)?pC(g)+qD(g),如图所示是A的转化率同压强,温度的关系,分析图象可以得出的正确结论是( )| A. | 正反应吸热,m+n<ρ+q | B. | 正反应吸热,m+n>ρ+q | ||
| C. | 正反应放热,m+n<ρ+q | D. | 正反应放热:m+n>ρ+q |
| A. | 60% | B. | 70% | C. | 80% | D. | 90% |
| A. | 加入稀盐酸产生气体,将气体通入澄清石灰水,溶液变浑浊,一定有CO32- | |
| B. | 加入氢氧化钠溶液共热产生使润湿的红色石蕊试纸变蓝的气体,一定有NH4+ | |
| C. | 加入氯化钡溶液有白色沉淀产生,再加盐酸,沉淀不消失,一定有SO42- | |
| D. | 加入氯水,再加KSCN溶液显红色,一定有Fe3+ |
| A. | 1 mol H2O | B. | 16 g O2 | C. | 1 mol Fe | D. | 2 g H2 |
| A. | 直径介于1 nm~100 nm之间的微粒称为胶体 | |
| B. | 制备Fe(OH)3胶体的方法是将饱和FeCl3溶液加热煮沸 | |
| C. | 利用丁达尔效应可以区分溶液和胶体 | |
| D. | 溶液、胶体与浊液的本质区别是其稳定性,胶体属于介稳体系 |
| A. | c (Na+)═c(CH3COO-)+c(CH3COOH) | B. | c(H+)═c(CH3COO-)+c(OH一) | ||
| C. | c (Na+)>c (CH3COO-)>c(OH-)>c(H+) | D. | c (CH3COO-)>c(Na+)>c(H+)>c(OH-) |