题目内容
【题目】随原子序数递增,八种短周期元素(用字母x等表示)原子半径的相对大小、最高正价或最低负价的变化如图所示。

根据判断出的元素回答问题:
(1)X的原子结构示意图为 ______________。
(2)比较d、e常见离子的半径大小(用化学式表示,下同):______> ;比较g、h的最高价氧化物对应水化物的酸性强弱: >_______。
(3)任选上述元素组成一种四原子共价化合物,写出其电子式:_____________。
【答案】 ![]() r(O2-) > r(Na+) HClO4 > H2SO4
r(O2-) > r(Na+) HClO4 > H2SO4 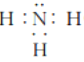 (或
(或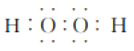 或
或![]() )
)
【解析】8种元素为短周期元素,在同一周期中,从左向右原子半径逐渐变小,同一主族,从上到下原子半径逐渐变小,主族元素最高正化合价一般等于族序数,最低负价=8-主族族序数,从图中的化合价、原子半径的大小及原子序数,可知x是H元素,y是C元素,z是N元素,d是O元素,e是Na元素,f是Al元素,g是S元素,h是Cl元素;根据以上分析解答。
(1)X是H元素,核电荷数为1, 原子结构示意图为 ![]() ;正确答案:
;正确答案:![]() 。
。
(2)电子层结构相同的离子,核电荷数越大离子半径越小,故离子半径:r(O2-)>r(Na+);非金属性越强,最高价氧化物水化物的酸性越强,故酸性:HClO4>H2SO4;正确答案:r(O2-) > r(Na+) ; HClO4 > H2SO4 。
(3)四原子共价化合物,可以是NH3、H2O2、C2H2等,其电子式为: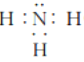 (或
(或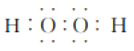
![]() 等);正确答案:
等);正确答案: (或
(或 或
或![]() )。
)。

练习册系列答案
 阳光试卷单元测试卷系列答案
阳光试卷单元测试卷系列答案
相关题目