题目内容
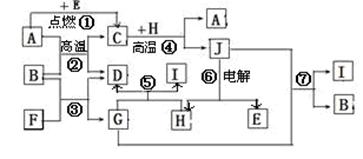
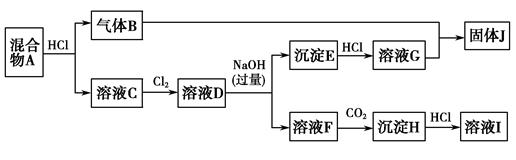
(10分)A为两种固体的混合物,G和I为溶液D的组成成分,E为红褐色沉淀,J为淡黄色固体。反应所加的试剂均足量。
(1)混合物A一定含有的元素为(写元素符号) ;
(2)溶液F一定含有的阴离子为(写离子符号) ;
(3)写出B+G―→J的化学方程式:
写出溶液C―→溶液D的离子方程式: ;
(4)I溶液I中溶质的阳离子常作净水剂,其作用原理是(用离子方程式表示):
。

(1)混合物A一定含有的元素为(写元素符号) ;
(2)溶液F一定含有的阴离子为(写离子符号) ;
(3)写出B+G―→J的化学方程式:
写出溶液C―→溶液D的离子方程式: ;
(4)I溶液I中溶质的阳离子常作净水剂,其作用原理是(用离子方程式表示):
。
(1)Fe、Al、S (2)Cl-、OH-、AlO (3)H2S+2FeCl3===2FeCl2+S↓+2HCl 2Fe2++Cl2===2Fe3++2Cl- (4)Al3++3H2O=Al(OH)3+3H+
由E为红褐色沉淀可它为Fe(OH)3,溶液G为FeCl3;溶液I中溶质的阳离子常作净水剂,说明溶液I的溶质为AlCl3,即溶液D的成分为FeCl3、AlCl3。而溶液C经和氯气氧化可得到溶液D,即2Fe2++Cl2===2Fe3++2Cl-,溶液C的成分为FeCl2、AlCl3。
J为淡黄色固体一定是硫,它可由FeCl3和气体B反应得到,说明B为H2S,即:H2S+2FeCl3===2FeCl2+S↓+2HCl。
最终可知混合物A中必含Fe、Al、S三种元素。
J为淡黄色固体一定是硫,它可由FeCl3和气体B反应得到,说明B为H2S,即:H2S+2FeCl3===2FeCl2+S↓+2HCl。
最终可知混合物A中必含Fe、Al、S三种元素。

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目