��Ŀ����
13����Ȼ��Ŀ����ʯ�ij���ͱ仯�ܵ�����������Ӱ�죮�ؿ���ÿ����1km��ѹǿ����Լ25000��30000kPa���ڵؿ���SiO2��HF��������ƽ�⣺SiO2��s��+4HF��g���TSiF4��g��+2H2O��g��+148.9kJ�����������������գ�
��1���ڵؿ��������SiF4��H2O�����ݳ����ڵؿ�dz��������SiO2������
��2�����������Ӧ��ƽ�ⳣ��Kֵ��÷�Ӧa��d��ѡ���ţ���
a��һ��������Ӧ�����ƶ� b����ƽ���ƶ�ʱ����Ӧ������������С
c��һ�����淴Ӧ�����ƶ� d����ƽ���ƶ�ʱ�淴Ӧ�����ȼ�С������
��3�����������Ӧ�����������ܱ������з���������Ӧ�ﵽƽ��ʱ��bc��ѡ���ţ���
a��2v����HF��=v����H2O�� b��v��H2O��=2v��SiF4��
c��SiO2���������ֲ��� d����Ӧ�ﲻ��ת��Ϊ������
��4������Ӧ�������ݻ�Ϊ2.0L����Ӧʱ��8.0min��������������ܶ�������0.12g/L�������ʱ����HF��ƽ����Ӧ����Ϊ0.0010mol/��L•min����
���� ��1��SiO2��s��+4HF��g��?SiF4��g��+2H2O��g��+148.9kJ�÷�ӦΪ����Ӧ�����С�ķ�Ӧ���ؿ���͵ؿ�dz��ʵ����ѹǿ�ĸı䣻
��2����ѧƽ�ⳣ��ֻ���¶ȵı仯���仯���÷�ӦΪ���ȷ�Ӧ��ƽ�ⳣ��Kֵ���˵���¶Ƚ���ƽ�����ƣ�
��3������Ӧ�ﵽƽ��ʱ������Ӧ����=�淴Ӧ�����Ҹ����ʵ�Ũ�ȱ��ֲ��䣬�ɴ˷�������ѡ�
��4����������ʽ����HF�ı仯����Ȼ�����v=$\frac{��c}{��t}$�����м�����⣮
��� �⣺��1��SiO2��s��+4HF��g��?SiF4��g��+2H2O��g��+148.9kJ�÷�ӦΪ����Ӧ�����С�ķ�Ӧ������ѹǿ��ƽ�������ƶ�����SiF4��g���ݳ���H2O��g������Ϊˮ����Сѹǿ��SiO2��s���������������ڵؿ��������SiF4��H2O �����ݳ����ڵؿ�dz�������� SiO2�������ʴ�Ϊ��SiF4��H2O��SiO2��
��2����ѧƽ�ⳣ��ֻ���¶ȵı仯���仯���÷�ӦΪ���ȷ�Ӧ��ƽ�ⳣ��Kֵ���˵���¶Ƚ���ƽ�����ƣ��¶Ƚ��ͷ�Ӧ���ʼ�С��ƽ�������淴Ӧ��������ѡ��a��d��
��3������Ӧ�ﵽƽ��ʱ������Ӧ����=�淴Ӧ�����Ҹ����ʵ�Ũ�ȱ��ֲ��䣻
a�����ݷ�Ӧ����֮�ȵ���ϵ��֮�ȿ��Եó���v����HF��=2v����H2O��������Ӧ�ﵽƽ��ʱ��v����H2O��=v����H2O�������v����HF��=2v����H2O�������a����
b�����ݷ�Ӧ����֮�ȵ���ϵ��֮�ȿ��Եó������ܷ�Ӧ��û�дﵽƽ�⣬����v����H2O��=2v����SiF4����v����H2O��=2v����SiF4��������Ӧ�ﵽƽ��ʱ��v����H2O��=v����H2O����v����SiF4��=v����SiF4������v����H2O��=2v����SiF4����v����H2O��=2v����SiF4������˲��ܷ�Ӧ��û�дﵽƽ�⣬v��H2O��=2v��SiF4������������b��ȷ��
c��SiO2���������ֲ���˵����Ӧ�Ѿ��ﵽƽ�⣬��c��ȷ��
d����Ӧ�ﵽƽ��ʱ���淴Ӧ��Ȼ���ڽ��У���Ӧ����������ڻ���ת����ֻ��������ȣ���d����ѡbc��
��4�����ݻ�Ϊ2.0L����Ӧʱ��8.0min��������������ܶ�������0.12g/L��
�����ӵ�����Ϊ2.0L��0.12g/L=0.24g���ɷ�Ӧ��Ԫ���غ��֪��ÿ4molHF��Ӧ������������28+16��2=60g��
��μӷ�Ӧ��HF��������Ϊx��
SiO2��s��+4HF��g��?SiF4��g��+2H2O��g����m
4mol 1mol 2mol 60g
x 0.24g
$\frac{4mol}{x}=\frac{60g}{0.24g}$�����x=0.016mol��
v��HF��=$\frac{��c}{��t}$=$\frac{\frac{0.016mol}{2L}}{8.0min}$=0.0010mol/��L•min��
�ʴ�Ϊ��0.0010mol/��L•min����
���� ��ѧ��Ӧ���ʺͻ�ѧƽ���ǻ�ѧ�������۵ĺ���֪ʶ��������ؿ������ݣ��ر����йػ�ѧ��Ӧ���ʺͻ�ѧƽ��ļ��㼰Ӱ�����ء���ѧƽ�ⳣ���ı���ʽ��������Ǹ߿����ص㣮

 ����ѧ��ţ��Ӣ��ϵ�д�
����ѧ��ţ��Ӣ��ϵ�д� ��ѧ�̸̳����¿α�ϵ�д�
��ѧ�̸̳����¿α�ϵ�д�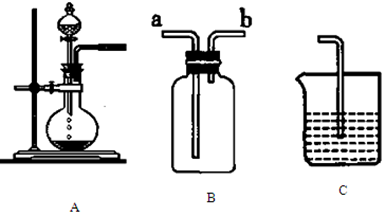
��1��װ��A�������Ʊ��������壬��д����Aװ���Ʊ���������ʱ��Բ����ƿ�ͷ�Һ©����Ӧװ�Ļ�ѧ�Լ�
| ���� | O2 | CO2 | HCl |
| �Լ� |
��3����Ҫ������װ����ȡCl2�������ʵ��Ƚ�Cl2��I2��������ǿ�������ڱ������������������װ�ú��Լ����ɲ�������
| װ�� | ��װ���з�Ӧ�����ӷ���ʽ |
| A�� | �������� | B�� | ������ | C�� | ���ᱵ | D�� | �������� |
| A�� | FeCl2 | B�� | CuCl2 | C�� | FeCl3 | D�� | AlCl3 |
| A�� | �����������������ʯӢ���ά | |
| B�� | �������ƿ����ڷ�ֹʳƷ�������ʣ��ӳ�ʳƷ�ı����� | |
| C�� | ̼�����������մ������������ͷۺ�����θ������ҩ�� | |
| D�� | ������������������ɫ�����Ϳ�� |
| A�� | c��NH4+����ȵģ�NH4��2SO4��Һ����NH4��2CO3��Һ��NH4Cl��Һ��c[��NH4��2CO3]��c[��NH4��2SO4]��c��NH4Cl�� | |
| B�� | pH��ȵ�CH3COONa��NaOH��Na2CO3������Һ��c��NaOH����c��CH3COONa����c��Na2CO3�� | |
| C�� | �ȵ����ʵ�����CH3COOH��CH3COONa�Ļ����Һ��c��CH3COO-��+2c��OH-��=2c��H+��+c��CH3COOH�� | |
| D�� | 0.1 mol•L-1 pH=4��NaHA��Һ�У�c��HA-����c��H+����c��H2A����c��A2-�� |
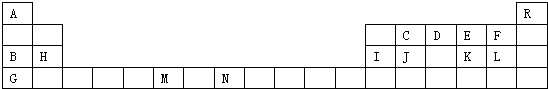
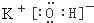 ��
�� ��
��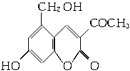 2006��5�£���������ڶ���ҩ�������ļ�ҩ����������ע��Һ�����¶�������������˥�ߣ����������ء��Ľṹ��ʽ��ͼ�������Ը��ϱ������ܳ���������ٴ�����ҩ��ʹ�����۵Ķ��ʴ���Ϊ���ϣ����ʴ�Ϊ��ҵ�ܼ����к�ǿ�Ķ��ԣ���ش��������⣺
2006��5�£���������ڶ���ҩ�������ļ�ҩ����������ע��Һ�����¶�������������˥�ߣ����������ء��Ľṹ��ʽ��ͼ�������Ը��ϱ������ܳ���������ٴ�����ҩ��ʹ�����۵Ķ��ʴ���Ϊ���ϣ����ʴ�Ϊ��ҵ�ܼ����к�ǿ�Ķ��ԣ���ش��������⣺