题目内容
已知:H2(g) + F2(g) = 2HF(g) ΔH=? 270 kJ/mol,下列说法正确的是
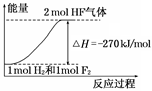
| A.在相同条件下,1 mol H2与1 mol F2的能量总和大于2 mol HF气体的能量 |
| B.1 mol H2与1 mol F2反应生成2 mol液态HF放出的热量小于270 kJ |
| C.该反应的逆反应是放热反应 |
| D.该反应过程的能量变化可用下图来表示 |

A
试题分析:A、ΔH=E生-E反?0 E生?E反,所以反应物:1 mol H2与1 mol F2的能量大于生成物:2 mol HF的能量,正确;B、2 mol液态HF的能量低于2 mol HF气体的能量,放出的热量大于270 kJ,错误;C、该反应的逆反应是吸热反应,错误;D、反应物:1 mol H2与1 mol F2的能量大于生成物:2 mol HF的能量, 错误。

练习册系列答案
相关题目
 2NH3(g)△H=-92.4 kJ·mol-1热化学方程式可知, 当反应中转移6NA电子时,反应放出的热小于92.4 kJ
2NH3(g)△H=-92.4 kJ·mol-1热化学方程式可知, 当反应中转移6NA电子时,反应放出的热小于92.4 kJ
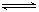 3O2 ;O3
3O2 ;O3
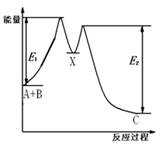
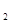 ·8H
·8H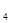 Cl晶体一起放入小烧杯中,将烧杯放在滴有3~4滴水的玻璃片上,用玻璃棒迅速搅拌。则下列说法正确的是
Cl晶体一起放入小烧杯中,将烧杯放在滴有3~4滴水的玻璃片上,用玻璃棒迅速搅拌。则下列说法正确的是 2HI(g) ΔH =-9.48 kJ·mol-1
2HI(g) ΔH =-9.48 kJ·mol-1