题目内容
利用电解法可将含有Fe、Zn、Ag、Pt等杂质的粗铜提纯,
下列叙述正确的是
| A.电解时可以精铜为阳极,以CuSO4溶液为电解液 |
| B.电解时阴极发生还原反应 |
| C.粗铜连接电源负极,其电极反应是Cu-2e—=Cu2+ |
| D.电解结束后,电解质溶液的浓度保持不变 |
B
解析试题分析:A选项,点解时,粗铜为阳极。B选项,正确。C选项,粗铜连接电源正极。D选项,电解结束后电解质溶液的浓度变低。
考点:电解池原理。

练习册系列答案
 口算能手系列答案
口算能手系列答案
相关题目
某汽车尾气分析仪以燃料电池为工作原理测定CO的浓度,其装置如图所示(上端为多孔电极a,下断为多孔电极b),该电池中电解质为氧化钇-氧化钠,其中O2-可以在固体介质NASICON中自由移动。下列说法不正确的是
| A.工作时电极b作正极,O2-由电极b流向电极a |
| B.工作时电子由电极a通过介质流向电极b |
| C.负极的电极反应式为:CO+O2—―2e-=CO2 |
| D.传感器中通过的电流越大,尾气中CO的含量越高 |
某固体酸燃料电池以CsHSO4固体为电解质传递H+,其基本结构见下图,电池总反应可表示为:2H2+O2=2H2O,下列有关说法正确的是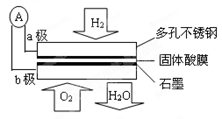
| A.电子通过外电路从b极流向a极 |
| B.每转移0.1mol电子,消耗1.12L的H2 |
| C.b极上的电极反应式为:O2 + 2H2O + 4e-= 4OH- |
| D.H+由a极通过固体酸膜电解质传递到b极 |
如图为番茄电池,下列有关说法中不正确的是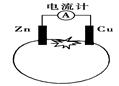
| A.一段时间后,铜电极附近会出现蓝色 |
| B.一段时间后,锌片质量会变少 |
| C.锌电极是该电池的负极 |
| D.电流由铜通过导线流向锌 |
下图所示的电解池I和II中,a、b、c和d均为Pt电极。电解过程中,电极b和d上没有气体逸出,但质量均增大,且增重b<d。符合上述实验结果的盐溶液是
| 选项 | X | Y |
| A. | MgSO4 | CuSO4 |
| B. | AgNO3 | Pb(NO3)2 |
| C. | FeSO4 | Al2 (SO4)3 |
| D. | CuSO4 | AgNO3 |
汽车的启动电源常用铅蓄电池,放电时的电池反应如下:PbO2 +Pb+2H2SO4=2PbSO4+2H2O,根据此反应判断下列叙述中正确的是
| A.PbO2是电池的负极 | B.负极的电极反应式为:Pb+SO42--2e– = PbSO4 |
| C.PbO2得电子,被氧化 | D.电池放电时,溶液酸性增强 |
用如图装置实验,下列叙述不正确的是( )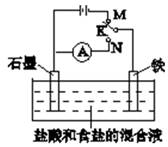
| A.K与N连接时,组成原电池装置 |
| B.K与N连接时,石墨电极产生气泡 |
| C.K与M连接时,一段时间后溶液的pH增小 |
| D.K与M连接时,石墨电极的反应为:2Cl--2e-=Cl2↑ |
下列关于金属腐蚀与防护的说法不正确的是
| A.金属腐蚀就是金属失去电子被氧化的过程。 |
| B.铝制品的耐腐蚀性强,说明铝的化学性质不活泼 |
| C.将海水中钢铁闸门与电源的负极相连,可防止闸门被腐蚀 |
| D.铁在NaOH和NaNO2的混合液中发蓝、发黑,使铁表面生成一层致密的氧化膜Fe3O4,防止钢铁腐蚀,其反应为:9Fe+8H2O+4NaNO2=3Fe3O4+4NH3↑+4NaOH |
要在铁制品上镀上一定厚度的锌层,以下设计方案正确的是( )
| A.锌作阳极,铁制品作阴极,溶液含有锌离子 |
| B.铂作阴极,铁制品作阳极,溶液含有锌离子 |
| C.铁作阳极,铁制品作阴极,溶液含有亚铁离子 |
| D.锌用阴极,铁制品作阳极,溶液含有锌离子 |