题目内容
(4分)室温下,将铁片、铜片、铝片(表面用砂纸打磨过)分别投入浓盐酸、浓硫酸、浓硝酸、浓氢氧化钠溶液四种试剂中,做了12个实验,实验的编号如下表所示。
|
|
浓盐酸 |
浓硫酸 |
浓硝酸 |
浓氢氧化钠溶液 |
|
铝 |
实验1 |
实验2 |
实验3 |
实验4 |
|
铁 |
实验5 |
实验6 |
实验7 |
实验8 |
|
铜 |
实验9 |
实验1O |
实验11 |
实验12 |
回答有关上述实验的下列问题:
(1) 若给以上溶液加热,也不会发生化学反应的实验是 和12(填实验编号)。
(2) 写出实验4发生的离子方程式 。
(4分)(1)8、9(2)2Al+2OH—+2H2O=2AlO2—+3H2↑
【解析】

(4分)室温下,将铁片、铜片、铝片(表面用砂纸打磨过)分别投入浓盐酸、浓硫酸、浓硝酸、浓氢氧化钠溶液四种试剂中,做了12个实验,实验的编号如下表所示。
|
| 浓盐酸 | 浓硫酸 | 浓硝酸 | 浓氢氧化钠溶液 |
| 铝 | 实验1 | 实验2 | 实验3 | 实验4 |
| 铁 | 实验5 | 实验6 | 实验7 | 实验8 |
| 铜 | 实验9 | 实验1O | 实验11 | 实验12 |
回答有关上述实验的下列问题:
(1) 若给以上溶液加热,也不会发生化学反应的实验是 和12(填实验编号)。
(2) 写出实验4发生的离子方程式 。
[2012·云南省质检](10分)用如图所示装置测定Fe和Fe2O3的混合物中单质铁的质量分数(夹持部分已略去)。称取Wg样品置于锥形瓶中,通过分液漏斗加入足量稀硫酸使样品完全溶解。实验前量气管起始读数为amL,实验后量气管的最终读数为bmL。
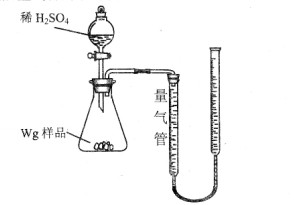
请回答下列问题:
(1)按上图完成装置连接,开始实验前必须进行的操作是 。
(2)写出锥形瓶中发生化合反应的离子方程式: 。
(3)实验结束后,锥形瓶内溶液中存在的金属离子有哪些可能?请根据选项进行填空(表格不一定填完):
A.盐酸 B.KSCN溶液 C.酸性KMnO4溶液 D.H2O2溶液
|
序号 |
溶液中可能存在 的金属离子 |
选择最少种数的试剂,验证该 假设(填字母) |
|
① |
|
|
|
② |
|
|
|
③ |
|
|
(4)实验中要对量气管多次读数,读数时应注意:①将实验装置恢复到室温;② ; ③视线与凹液面最低处相平。若读取量气管中气体的体积时,液面左高右低,则所测气体的体积 (填“偏大”、“偏小”或“无影响’”)。
(5)若样品与足量稀硫酸反应后滴入KSCN溶液不显红色且量气管读数b>a(该实验条件下的气体摩尔体积为Vm)。下列有关单质铁质量分数的计算过程是否正确? (填“是”或“否”), 理由是 。
Fe+H2SO4=FeSO4+H2↑
56g VmL
Wg× (Fe)
(b-a)×10-3L
(Fe)
(b-a)×10-3L
……

(10分)室温下,将铁片、铜片、铝片(表面用砂纸打磨过)分别投入浓盐酸、浓硫酸、浓硝酸、浓氢氧化钠溶液四种试剂中,做了12个实验,实验的编号如下表所示。
| 浓盐酸 | 浓硫酸 | 浓硝酸 | 浓氢氧化钠溶液 |
铝 | 实验1 | 实验2 | 实验3 | 实验4 |
铁 | 实验5 | 实验6 | 实验7 | 实验8 |
铜 | 实验9 | 实验1O | 实验11 | 实验12 |
回答有关上述实验的下列问题:
(1)三种金属投入以上某种试剂中均无明显现象,这种试剂是 。
(2)有一个实验最能直观证明硝酸具有强氧化性,该实验的编号是 。
(3)能说明金属遇浓硫酸会发生“钝化”现象的实验是 (填实验编号)。
(4)若给以上溶液加热,也不会发生化学反应的实验是 和12(填实验编号)。
(5)写出实验4发生的化学方程式 。
 。
。