题目内容
【题目】类比pH的定义,对于稀溶液可以定义pC=-lgC,pKa=-lgKa。常温下,某浓度H2A溶液中滴加NaOH溶液,测得pC(H2A)、pC(HA-)、pC(A2-)变化如图所示。下列说法正确的是()
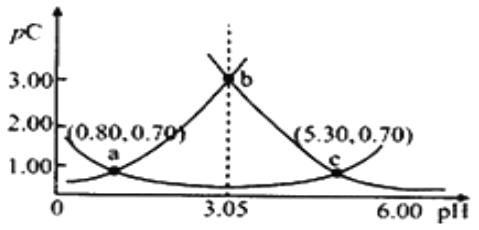
A. pH=3.50时,c(H2A)>c(HA-)>c(A2-)
B. 从a点开始滴入NaOH溶液,溶液中c(H+)/c(H2A)先减小后增大
C. 将等浓度等体积的Na2A与H2A溶液混合后,溶液显碱性
D. pH从3.00到5.30时,c(H2A)+c(HA-)+c(A2-)先增大后减小
【答案】B
【解析】
根据H2A![]() H++HA-,HA-
H++HA-,HA-![]() H++ A2-,pH变化时,HA-的浓度变化不大,因此,pC变化幅度不大的曲线,即图中随着pH的增大,pC先减小后增大的曲线是HA-的物质的量浓度的负对数;pH越大,c(H+)越小,则电离平衡正向移动程度越大,所以由图可知,随着pH的增大,pC增大的曲线是H2A的物质的量浓度的负对数,随着pH的增大,pC减小的曲线是A2-的物质的量浓度的负对数,据此答题。
H++ A2-,pH变化时,HA-的浓度变化不大,因此,pC变化幅度不大的曲线,即图中随着pH的增大,pC先减小后增大的曲线是HA-的物质的量浓度的负对数;pH越大,c(H+)越小,则电离平衡正向移动程度越大,所以由图可知,随着pH的增大,pC增大的曲线是H2A的物质的量浓度的负对数,随着pH的增大,pC减小的曲线是A2-的物质的量浓度的负对数,据此答题。
A.pH=3.50时,pC(A2-)> pC(HA-),所以c(HA-)>c(A2-)>c(H2A),故A错误;
B.一开始滴入NaOH溶液,H+与OH-不断中和,故c(H+)/c(H2A)减小,反应一段时间后,H2A不断电离,浓度减小,H+的浓度越来越大,故c(H+)/c(H2A)增大,故B正确;
C.将等浓度等体积的Na2A与H2A溶液混合后生成NaHA,由图像可知,HA-的电离程度大于水解程度,溶液呈酸性,故C错误;
D.根据物料守恒,c(H2A)+c(HA-)+c(A2-)始终不变,故D错误。
故选B。

练习册系列答案
相关题目