题目内容
在pH=1的溶液中能大量共存的一组离子或分子是( )
| A.Al3+、NH4+、Br-、Cl- |
| B.Na+、Mg2+、ClO-、NO3- |
| C.K+、MnO4-、CH3CHO、SO42- |
| D.Na+、K+、SiO32-、Cl- |
A
解析

练习册系列答案
 数学奥赛暑假天天练南京大学出版社系列答案
数学奥赛暑假天天练南京大学出版社系列答案 南大教辅抢先起跑暑假衔接教程南京大学出版社系列答案
南大教辅抢先起跑暑假衔接教程南京大学出版社系列答案
相关题目
下列离子在溶液中因发生氧化还原反应而不能大量共存的是
| A.H+、NO3—、Fe2+、Na+ | B.Ag+、NO3—、C1—、K+ |
| C.K+、Ba2+、OH—、SO42— | D.Cu2+、NH4+、Br—、OH— |
下列离子方程式正确的是
| A.水玻璃长时间放置在空气中:SiO32-+CO2+H2O=H2SiO3↓+HCO3- |
| B.硫酸铜溶液显酸性:Cu2++2H2O=Cu(OH)2↓+2H+ |
C.用石墨电极电解饱和食盐水:2H++2Cl-  H2↑+Cl2↑ H2↑+Cl2↑ |
| D.向明矾溶液中滴加Ba(OH)2溶液,恰好使SO42-沉淀完全: |
常温下,下列各组离子在指定溶液中一定能大量共存的是
| A.使石蕊试液变红的溶液中:I-、K+、NO3—、Na+ |
| B.含有大量Fe3+的溶液:NH4+、HCO3—、SO42—、OH— |
| C.水电离出c(H+)=1.0×10-12mol/L的溶液:Cl-、Na+、ClO-、NH4+ |
| D.澄清透明的溶液:Cu2+、Fe3+、SO42—、NO3— |
下列过程的离子方程式正确的是
| A.用烧碱溶液吸收Cl2:Cl2+2OH- =Cl-+ClO-+H2O |
| B.用饱和Na2CO3溶液转化锅垢中的CaSO4:CaSO4(s)+CO32- (aq)=CaCO3(s)+SO42-(aq) |
| C.实验室制备Fe(OH)3胶体:Fe3+ +3OH- =Fe(OH)3↓ |
| D.金属Na与水反应:Na +2H+ = H2↑+Na+ |
室温时,下列各组离子在指定溶液中可以大量共存的是
A.由水电离出的c(H+)=10-12mol/L的溶液中:Na+、Ba2+、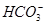 、Cl- 、Cl- |
| B.无色透明溶液中:K+、Cu2+、SO42-、Na+ |
C.含有大量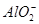 的溶液中:Na+、OH-、Cl-、 的溶液中:Na+、OH-、Cl-、 |
D.能使pH试纸显红色的溶液中:Na+、ClO-、Fe2+、 |
下列各溶液中,一定能大量共存的离子组是( )
| A.室温下,由水电离出c(OH-)=1×10-12 mol·L-1的溶液中:K+、HCO3-、Na+、Cl- |
| B.含有0.1 mol·L-1 Fe2+的溶液中:NH4+、SO42-、H+、NO3- |
| C.澄清透明的溶液中:Cu2+、Mg2+、SO42-、Cl- |
| D.室温下,pH=1的溶液中:Na+、Cl-、K+、CH3COO- |
下列离子方程式与所述事实相符且正确的是( )
| A.漂白粉溶液在空气中失效:ClO-+CO2+H2O=HClO+HCO3- |
B.用浓盐酸与MnO2反应制取少量氯气:MnO2+2H++2Cl- Mn2++Cl2↑+2H2O Mn2++Cl2↑+2H2O |
| C.向NaAlO2溶液中通入过量CO2制Al(OH)3:AlO2-+CO2+2H2O=Al(OH)3↓+HCO3- |
| D.在强碱溶液中次氯酸钠与Fe(OH)3反应生成Na2FeO4:3ClO-+2Fe(OH)3=2FeO42-+3Cl-+H2O+4H+ |
下列有关物质检验的实验结论正确的是
| | 实验操作 | 现象 | 实验结论 |
| A | 向某溶液中加入盐酸酸化的氯化钡溶液 | 有白色沉淀生成 | 溶液中一定含有 |
| B | 将某气体通入澄清石灰水中 | 变浑浊 | 该气体一定是CO2 |
| C | 向某溶液中加入2滴KSCN溶液 | 溶液不显红色 | 溶液中一定含有Fe2+ |
| 另取样,先滴入氯水,再滴入KSCN溶液 | 溶液变为红色 | ||
| D | 将少量某物质的溶液滴加到新制的银氨溶液中,水浴加热 | 有银镜生成 | 该物质一定是葡萄糖 |