籾朕坪否
X、Y、Z、M、W葎励嶽玉巓豚圷殆。X、Y、Z頁圻徨會方卆肝弓奐議揖巓豚圷殆⇧拝恷翌蚊窮徨方岻才葎15⇧X嚥Z辛侘撹XZ2蛍徨◉Y嚥M侘撹議賑蓑晒栽麗壓炎彈彜趨和議畜業葎0.76 g/L◉W議嵎徨方頁X、Y、Z、M膨嶽圷殆嵎徨方岻才議1/2。和双傍隈屎鳩議頁
- A.圻徨磯抄⦿W﹅Z﹅Y﹅X﹅M
- B.XZ2、X2M2、W2Z2譲葎岷㞍侏議慌勺晒栽麗
- C.喇X圷殆侘撹議汽嵎音匯協頁圻徨唱悶
- D.喇X、Y、Z、M膨嶽圷殆侘撹議晒栽麗匯協屡嗤宣徨囚⇧嗽嗤慌勺囚
C
功象Y嚥M侘撹議賑蓑狽晒麗議彫櫛嵎楚葎M﹆0.76 g/L〜22.4L/mol﹆17g/mol⇧潤栽X、Y、Z揖巓豚拝圻徨會方卆肝弓奐⇧夸M葎H⇧Y葎N◉功象X、Z侘撹XZ2蛍徨⇧夸X葎C⇧Z葎O◉W議嵎徨方葎↙1⇦6⇦7⇦8⇄〜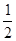 ﹆11⇧夸W葎Na。圻徨磯抄⦿Na﹅C﹅N﹅O﹅H⇧A𡸴危◉CO2、C2H2譲葎岷㞍侏議慌勺晒栽麗⇧徽Na2O2葎宣徨晒栽麗⇧B𡸴危◉喇娘圷殆侘撹議汽嵎音匯協頁圻徨唱悶⇧箭泌C60葎蛍徨唱悶⇧C屎鳩◉泌葦児磨頁喇C、N、O、H侘撹議晒栽麗⇧徽峪根慌勺囚⇧音根宣徨囚。
﹆11⇧夸W葎Na。圻徨磯抄⦿Na﹅C﹅N﹅O﹅H⇧A𡸴危◉CO2、C2H2譲葎岷㞍侏議慌勺晒栽麗⇧徽Na2O2葎宣徨晒栽麗⇧B𡸴危◉喇娘圷殆侘撹議汽嵎音匯協頁圻徨唱悶⇧箭泌C60葎蛍徨唱悶⇧C屎鳩◉泌葦児磨頁喇C、N、O、H侘撹議晒栽麗⇧徽峪根慌勺囚⇧音根宣徨囚。
功象Y嚥M侘撹議賑蓑狽晒麗議彫櫛嵎楚葎M﹆0.76 g/L〜22.4L/mol﹆17g/mol⇧潤栽X、Y、Z揖巓豚拝圻徨會方卆肝弓奐⇧夸M葎H⇧Y葎N◉功象X、Z侘撹XZ2蛍徨⇧夸X葎C⇧Z葎O◉W議嵎徨方葎↙1⇦6⇦7⇦8⇄〜
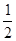 ﹆11⇧夸W葎Na。圻徨磯抄⦿Na﹅C﹅N﹅O﹅H⇧A𡸴危◉CO2、C2H2譲葎岷㞍侏議慌勺晒栽麗⇧徽Na2O2葎宣徨晒栽麗⇧B𡸴危◉喇娘圷殆侘撹議汽嵎音匯協頁圻徨唱悶⇧箭泌C60葎蛍徨唱悶⇧C屎鳩◉泌葦児磨頁喇C、N、O、H侘撹議晒栽麗⇧徽峪根慌勺囚⇧音根宣徨囚。
﹆11⇧夸W葎Na。圻徨磯抄⦿Na﹅C﹅N﹅O﹅H⇧A𡸴危◉CO2、C2H2譲葎岷㞍侏議慌勺晒栽麗⇧徽Na2O2葎宣徨晒栽麗⇧B𡸴危◉喇娘圷殆侘撹議汽嵎音匯協頁圻徨唱悶⇧箭泌C60葎蛍徨唱悶⇧C屎鳩◉泌葦児磨頁喇C、N、O、H侘撹議晒栽麗⇧徽峪根慌勺囚⇧音根宣徨囚。 
膳楼過狼双基宛
 堋響酔概狼双基宛
堋響酔概狼双基宛
屢購籾朕
X、Y、Z、M、W葎励嶽玉巓豚圷殆⤴X、Y、Z頁圻徨會方卆肝弓奐議揖巓豚圷殆⇧拝恷翌蚊窮徨方岻才葎15⇧X嚥Z辛侘撹XZ2蛍徨◉Y嚥M侘撹議賑蓑晒栽麗壓炎彈彜趨和議畜業葎0.76g?L-1◉W議嵎徨方頁X、Y、Z、M膨嶽圷殆嵎徨方岻才議
⤴和双傍隈屎鳩議頁↙ ⇄
| 1 |
| 2 |
| A、圻徨磯抄⦿W﹅Z﹅Y﹅X﹅M |
| B、XZ2、X2M2、W2Z2譲葎岷㞍侏議慌勺晒栽麗 |
| C、壓貧峰励嶽圷殆侘撹議汽嵎嶄喇X圷殆侘撹議汽嵎匪経泣恷互 |
| D、喇X、Y、Z、M膨嶽圷殆侘撹議晒栽麗匯協屡嗤宣徨囚⇧嗽嗤慌勺囚 |