题目内容
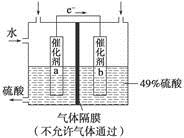
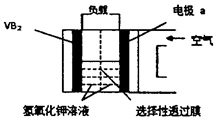
硼化钒-空气电池是目前储电能力最高的电池,电池示意图如下图所示,该电池工作时的反应为:4 VB2+11O2===4B2O3+2V2O5,下列说法正确的是
2 VB2+22OH-===V2O5+2B2O3+11H2O+22e-

| A.电极a是电源负极 |
| B.溶液中的OH-向a极移动 |
| C.电子由VB2极经KOH溶液流向电极a |
| D.VB2极发生的电极反应为: |
D
试题分析:空气中的O2是氧化剂,故a是电源正极,A错;正极反应式是2H2O+O2+4e-===4OH-,故OH-向b极移动;电子由VB2极经外电路流向电极a,溶液不导电子,C错;VB2极发生的电极反应用总反应减去2H2O+O2+4e-===4OH-,故D正确。

练习册系列答案
相关题目