��Ŀ����
����Ŀ��A��B��C��D����Ԫ�أ�ԭ��������������Aԭ�ӵ����������4�����ӣ�B�������Ӻ�C�������Ӿ�����ͬ�ĵ��Ӳ�ṹ����Ԫ�صĵ��ʷ�Ӧ������һ�ֵ���ɫ�Ĺ���E��D��L�����������K��M�������Ӳ��ϵĵ�����֮�ͣ�
��1��AΪ______��CΪ______������Ԫ�ط��ţ�
��2��д��A��B�Ļ�������E��Ӧ�Ļ�ѧ����ʽ��______��
��3��A��B��Ԫ���γɵĻ�������______������ӡ����ۡ��������
��4��д��D������������ˮ�����A���ʷ�Ӧ�Ļ�ѧ����ʽ��______��
���𰸡� C Na 2Na2O2+CO2=2Na2CO3+O2�� ���� C+2H2SO4��Ũ��![]() CO2��+2SO2��+2H2O
CO2��+2SO2��+2H2O
��������������A��B��C��DΪ���ֶ�����Ԫ�أ�ԭ��������������B�������Ӻ�C�������Ӿ�����ͬ�ĵ��Ӳ�ṹ����Ԫ�صĵ��ʷ�Ӧ������һ�ֵ���ɫ�Ĺ���E�������EΪNa2O2����BΪOԪ�ء�CΪNaԪ�أ�A��ԭ������С��B����Aԭ�ӵ����������4�����ӣ���AΪCԪ�أ�D��L�����������K��M�������Ӳ��ϵ�����֮�ͣ���Dԭ��M�������Ϊ8��2=6�����������ӷֱ�Ϊ2��8��6����DΪSԪ����
��1��������������֪��AΪCԪ�ء�CΪNaԪ�أ��ʴ�Ϊ��C��Na��
��2��A��B�Ļ�������E��Ӧ�Ƕ�����̼��������Ʒ�Ӧ����̼��������������ѧ��Ӧ����ʽΪ��2Na2O2+CO2=2Na2CO3+O2���ʴ�Ϊ��2Na2O2+CO2=2Na2CO3+O2��
��3��A��B��Ԫ���γɵĻ�����ΪCO��CO2�����ڹ��ۻ�����ʴ�Ϊ�����ۣ�
��4��D������������ˮ����Ϊ���ᣬ��̼��Ӧ�Ļ�ѧ����ʽ��C+2H2SO4��Ũ��![]() CO2��+2SO2��+2H2O���ʴ�Ϊ��C+2H2SO4��Ũ��
CO2��+2SO2��+2H2O���ʴ�Ϊ��C+2H2SO4��Ũ��![]() CO2��+2SO2��+2H2O��
CO2��+2SO2��+2H2O��

����Ŀ���±���Ԫ�����ڱ���һ���֣���ش��й����⣺
�� ���� | ��A | ��A | ��A | ��A | ��A | ��A | ��A | 0 |
2 | �� | �� | �� | |||||
3 | �� | �� | �� | �� | �� | |||
4 | �� | �� |
��1�����л�ѧ��������õ�Ԫ�أ���ԭ�ӽṹʾ��ͼΪ______��
��2���������γ��������������Ԫ����______ ����Ԫ�ط��ű�ʾ����д����Ԫ�صĵ����������������Ӧˮ���ﷴӦ�Ļ�ѧ����ʽ______��
��3�����ʵ�鷽�����ȽϢ���ⵥ�������Ե�ǿ�����뽫�����������___��
ʵ����������� | |
����Ŀ��ͭ����������;�㷺�Ľ�������ҵ�����õ�����ࣨ��Ҫ����Fe2O3��CuO��Cr2O3�������������ʣ����ս���ͭ����������ͼ�� 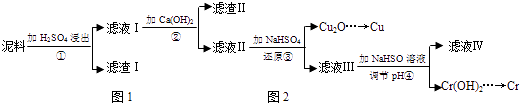
��֪���������ʳ�����pH�����
Fe3+ | Cu2+ | Cr3+ | |
��ʼ����pH | 2.1 | 4.7 | 4.3 |
��ȫ����pH | 3.2 | 6.7 | a |
��ش��������⣺
��1����ҺI������������Ҫ�����ѧʽ����
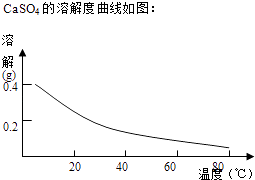
��2���ڢڲ������У��ȼ���Ca��OH��2������Һ��pH�����ڷ�ΧΪ �� Ȼ����Һ������80����ȹ��ˣ�����������ijɷ�Ϊ ��
��3��������Ũ�ȡ�1��10��5molL��1ʱ��������Ϊ���ӳ�����ȫ���ڢܲ������У���ҪʹCr3+��ȫ����������������Һ��a����СֵΪ �� ����֪��Kap[Cr��OH��3]=6.3��10��31 �� ![]() ��4.0��lg4=0.6��
��4.0��lg4=0.6��
��4��Cr��OH��3���ȷֽ�ΪCr2O3 �� �����ȷ�����ұ����������д�����ȷ������Ļ�ѧ����ʽ ��
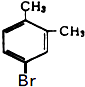
����Ŀ����֪���ױ���3��ͬ���칹�壬���ױ��б����ϵ�һ����ﹲ��6�֣����۵���±���
6��һ����ױ����۵�/�� | 234 | 206 | 213.8 | 204 | 214.5 | 205 |
��Ӧ���ױ����۵�/�� | 13 | ��54 | ��27 | ��54 | ��27 | ��54 |
�ɴ��ƶ��۵�Ϊ234���һ����ױ������ǣ� ��
A.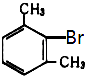
B.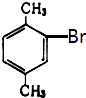
C.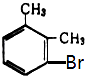
D.