题目内容
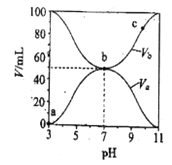
【题目】【曲靖市第一中学2017届质量监测考试(八)】常温下,向l0mL0.1mol/L的HR溶液中逐渐滴入0.lmol/L的NH3·H2O 溶液,所得溶液pH及导电性变化如图。下列分析不正确的是
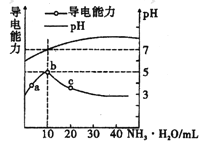
A.ab点导电能力增强,说明HR为弱酸
B.b点溶液,c(NH3H2O)=c(R-)+c(H+)-c(OH-)
C.c点溶液,存在c(NH4+)>c(R-)>c(OH-)>c(H+)
D.常温下,HR和NH3H2O的电离平衡常数相等
【答案】B
【解析】A.a~b点导电能力增强,说明反应后溶液中离子浓度增大,证明HR在溶液中部分电离,为弱酸,A正确;B.根据图象可知b点溶液pH=7,此时HR与一水合氨的物质的量相等,说明此时二者恰好反应生成NH4R,铵根离子与R-的水解程度相等,溶液呈中性,根据物料守恒c(NH3H2O)+c(NH4+)=c(R-)+c(HR),B错误;C.根据图象可知,c点时溶液的pH>7,混合液呈碱性,则c(NH4+)>c(R-)>c(OH-)>c(H+),C正确;D.根据B中分析可知常温下,HR和NH3H2O的电离平衡常数相等,D正确;答案选B。

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案【题目】【镇江市2017届三模(最后一卷)】α-氯乙基苯是一种重要的有机合成中间体,其一种制备反应原理为: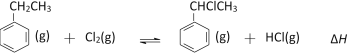
在T℃时,向2.0 L恒容密闭容器中充入0.40mol乙苯(g)和0.40mol Cl2(g)进行反应,反应过程中测定的部分数据见下表:
t/min | 0 | 1 | 2 | 5 | 10 |
n(HCl)/mol | 0 | 0.12 | 0.20 | 0.32 | 0.32 |
下列有关说法正确的是
A.反应在0~2 min内的平均速率v(α-氯乙基苯)=0.10mol·L-1·min-1
B.10 min后,若保持其他条件不变,升高温度,达到新平衡时测得c(α-氯乙基苯)=0.18mol·L-1,则反应的ΔH>0
C.在T℃时,起始时若向容器中充入1.0 mol乙苯(g)、0.50 mol Cl2(g)和0.50 mol α-氯乙基苯(g)、0.50 mol HCl(g),则反应将向正反应方向进行
D.在T℃时,起始时若向容器中充入2.0molα-氯乙基苯(g)和2.2mol HCl(g),达到平衡时,α-氯乙基苯(g)的转化率小于20%