题目内容
【题目】实验室测定铬铁矿中铬(Cr)含量的步骤如下:
步骤1:准确称取0.2000g铬铁矿试样放入锥形瓶中,加入适量磷酸和硫酸的混合酸,加热使试样完全溶解,冷却。
步骤2:向上述溶液中滴加5滴1%MnSO4溶液,再加入一定量的(NH4)2S2O8溶液,摇匀至溶液呈紫红色[先后发生Cr3+![]() Cr2O72-、Mn2+
Cr2O72-、Mn2+![]() MnO4-]。
MnO4-]。
步骤3:上述溶液加热煮沸至紫红色褪去[除去过量的(NH4)2S2O8和生成的MnO4-],冷却。
步骤4:用0.2000mol·L-1(NH4)2Fe(SO4)2标准溶液滴定上述溶液至终点(发生Cr2O72-![]() Cr3+),消耗19.50mL标准溶液。
Cr3+),消耗19.50mL标准溶液。
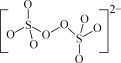
(1)(NH4)2S2O8中阴离子的结构如图所示。从结构分析,(NH4)2S2O8置于棕色试剂瓶并于阴凉处保存的原因是__。
(2)“步骤2”中加入5滴1%MnSO4溶液的目的是__。
(3)“步骤3”中,如果继续加热煮沸时间不充足,会使铬含量的测定结果___(填“偏大”“不变”或“偏小”)。
(4)计算铬铁矿中铬的质量分数___(写出计算过程)。
【答案】过氧键见光、受热易断裂而造成物质分解 判断溶液中的Cr3+是否完全被氧化成Cr2O72- 偏大 33.8%
【解析】
(1)棕色试剂瓶是存放见光易分解的物质;
(2)加入5滴MnSO4溶液的目的是作为Cr3+与(NH4)2S2O8反应的指示剂;
(3)“氧化”过程中,如果继续加热煮沸时间不充足,溶液中过量的(NH4)2S2O8和生成的HMnO4不能完全分解除去,会消耗更多(NH4)2Fe(SO4)2标准溶液;
(4)6Fe2++Cr2O72-+14H+=6Fe3++2Cr3++7H2O,得到:6Fe2+~Cr2O72-,结合操作过程中的定量关系计算。
(1)从结构分析,(NH4)2S2O8置于棕色试剂瓶并于阴凉处保存的原因是过氧键见光、受热易断裂而造成物质分解。
故答案为:过氧键见光、受热易断裂而造成物质分解;
(2)“步骤2”中加入5滴1%MnSO4溶液的目的是作为Cr3+与(NH4)2S2O8反应的指示剂,判断溶液中的Cr3+是否完全被氧化成Cr2O72-。
故答案为:判断溶液中的Cr3+是否完全被氧化成Cr2O72-;
(3)②“氧化”过程中,如果继续加热煮沸时间不充足,溶液中过量的(NH4)2S2O8和生成的HMnO4不能完全分解除去,会消耗更多(NH4)2Fe(SO4)2标准溶液,导致计算得到结果偏大;
故答案为:偏大;
(4)根据氧化还原反应规律:亚铁离子被氧化,离子方程式为:6Fe2++Cr2O72-+14H+=6Fe3++2Cr3++7H2O,据此得到:6Fe2+~Cr2O72-,n(Cr2O72-)=![]() ×0.20000mol·L-1×19.50mL×10-3 mL·L-1=6.5×10-4 mol,铬的质量分数=
×0.20000mol·L-1×19.50mL×10-3 mL·L-1=6.5×10-4 mol,铬的质量分数=![]() ×100%=33.8%;
×100%=33.8%;
故答案为:33.8%。

【题目】某实验小组对H2O2分解反应进行实验探究:将质量相等状态不同的MnO2分别加入盛有等体积等浓度的H2O2溶液的大试管中,并用带火星的木条在试管口测试。有关记录如下:
MnO2 | 触摸试管 | 现象 | 反应时间/min |
粉末 | 发烫 | 反应剧烈,带火星的木条迅速复燃 | t1 |
块状 | 微热 | 反应较慢,火星红亮但木条未复燃 | t2 |
(1)试管中化学反应方程式:____________。
(2)实验结果证明了催化剂的催化效果与____________有关。
(3)表中t1____________t2(填写“>”、“<”或“=”)
(4)控制该反应速率,除了改变催化剂因素,可行的方法还有____________。
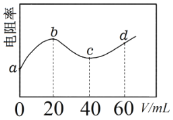
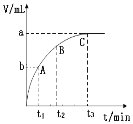
(5)某同学用一定浓度的H2O2溶液10mL,加入适量MnO2在某温度下反应,测量放出气体的体积(标准状况)与反应时间的关系如图所示,则A、B、C三点所表示的即时反应速率最慢的是____________点。
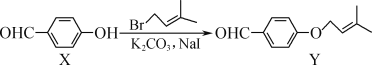
【题目】H2S是石油化工行业广泛存在的污染性气体,但同时也是重要的氢源和硫源,工业上可以采取多种方式处理。
Ⅰ.干法脱硫
(1)已知:2H2S(g)+3O2(g)=2SO2(g)+2H2O(l);ΔH1=akJ·mol-1
S(s)+O2(g)=SO2(g);ΔH2=bkJ·mol-1
则空气氧化脱除H2S反应2H2S(g)+O2(g)=2S(s)+2H2O(l)的ΔH=___kJ·mol-1。
(2)常用脱硫剂的脱硫效果及反应条件如表,则最佳脱硫剂为___。
脱硫剂 | 出口硫/(mg·m-3) | 脱硫温度/℃ | 操作压力(MPa) | 再生条件 |
一氧化碳 | <1.33 | 300~400 | 0~3.0 | 蒸汽再生 |
活性碳 | <1.33 | 常温 | 0~3.0 | 蒸汽再生 |
氧化锌 | <1.33 | 350~400 | 0~5.0 | 不再生 |
锌锰矿 | <3.99 | 400 | 0~2.0 | 不再生 |
Ⅱ.热分解法脱硫
在密闭容器中,充入一定量的H2S气体,发生如下热分解反应:H2S(g)![]() H2(g)+
H2(g)+![]() S2(g)
S2(g)
控制不同的温度和压强进行实验,结果如图1所示。
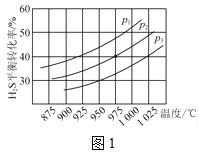
(1)p1、p2、p3由大到小的顺序为___。
()保持压强不变,能提高H2S的平衡转化率的措施有__(写一条)。
Ⅲ.间接电解法脱硫
间接电解法脱硫原理如图2所示(吸收反应器中盛放FeCl3溶液,电解反应器的阴极、阳极均为惰性电极)。
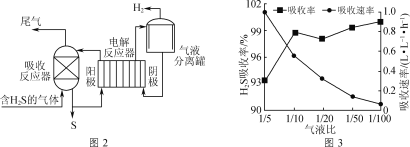
(1)吸收反应器中发生反应的离子方程式为___。
(2)反应器阴极生成H2的电极反应式为__。
(3)气液比为气体与液体的流速比,吸收反应器内液体流速固定。测定吸收器中相同时间内不同气液比下H2S的吸收率和吸收速率,结果如图3所示。随着气液比减小,H2S的吸收率呈上升趋势的原因为___。
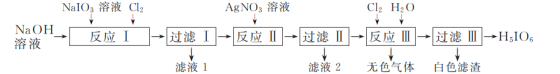
【题目】下列实验操作对应的现象不符合事实的是
|
|
|
|
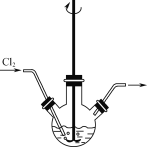
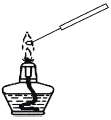
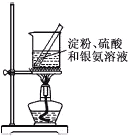
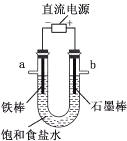
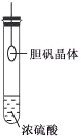
A.用铂丝蘸取NaCl溶液置于酒精灯火焰上灼烧,火焰呈黄色 | B.将少量银氨溶液加入盛有淀粉和硫酸的试管中,加热,产生光亮的银镜 | C.饱和食盐水通电一段时间后,湿润的KI-淀粉试纸遇b处气体变蓝色 | D.将胆矾晶体悬挂于盛有浓H2SO4的密闭试管中,蓝色晶体逐渐变为白色 |
A. A B. B C. C D. D