题目内容
【题目】为了探究三种气态氧化物(SO2、NO2、CO2)的性质,某同学设计了一组实验:
(1)实验一:探究三种气体在水中的溶解性,用三支相同的试管收集满三种气体,倒置在盛满水的烧杯中,一段时间后,观察到的现象如图A,B,C所示. 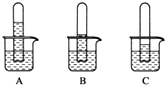
(i)在相同条件下,三种气体在水中溶解度最大的是 .
写出A烧杯中发生反应的化学方程式: .
(2)实验二:用三只集气瓶收集满二氧化硫、二氧化氮气体,然后将其倒置在水槽中.分别缓慢通入适量O2或Cl2 , 如图D,E,F所示.一段时间后,D,E装置的集气瓶中充满溶液,F装置的集气瓶中还有气体剩余. 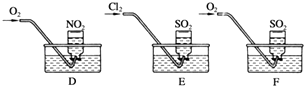
(ii)实验二中装置D的集气瓶最终充满溶液(假设瓶内液体不扩散):
①写出装置D中总反应的化学方程式: .
②假设该实验条件下,气体摩尔体积为a Lmol﹣1 . 则装置D的集气瓶中所得溶液溶质的物质的量浓度为 .
(iii)实验前在F装置的水槽里滴加几滴紫色石蕊试液,观察到的现象是 , 通入氧气后,可能观察到的实验现象是 , 写出反应的化学方程式: .
(iv)溶液充满集气瓶后,在E装置的水槽里滴加硝酸钡溶液,写出有关反应的离子方程式 .
【答案】
(1)NO2(或A);3NO2+H2O═2HNO3+NO
(2)4NO2+O2+2H2O═4HNO3;![]() mol/L;紫色石蕊试液变红;红色由浅变深;2SO2+O2+2H2O=2H2SO4;SO2+Cl2+2H2O=4H++SO42﹣+Cl﹣、SO42﹣+Ba2+=BaSO4↓
mol/L;紫色石蕊试液变红;红色由浅变深;2SO2+O2+2H2O=2H2SO4;SO2+Cl2+2H2O=4H++SO42﹣+Cl﹣、SO42﹣+Ba2+=BaSO4↓
【解析】解:(1)(i)从图A、B、C的实验结果分析,试管里液面上升越高,表明相同条件下气体在水中溶解度越大;根据A中剩余气体的体积可以判断是二氧化氮溶于水发生反应生成NO:3NO2+H2O═2HNO3+NO,故答案为:NO2(或A);3NO2+H2O═2HNO3+NO;(2)(ii)①装置D中发生的反应有:3NO2+H2O═2HNO3+NO、2NO+O2═2NO2 , 相加得总反应方程式:4NO2+O2+2H2O═4HNO3 , 故答案为:4NO2+O2+2H2O═4HNO3;②水会充满集气瓶,设集气瓶体积为VL,最后溶液的体积为VL,由4NO2+O2+2H2O═4HNO3知,n(NO2)=n(HNO3),则所得溶液溶质的物质的量浓度为c= ![]() =
= ![]() =
= ![]() mol/L,故答案为:
mol/L,故答案为: ![]() mol/L;(iii)F装置中二氧化硫与水反应生成亚硫酸,溶液显酸性,滴加几滴紫色石蕊试液,观察到的现象是紫色溶液变红,再通入氧气,发生2SO2+O2+2H2O=2H2SO4 , 酸性增强,红色由浅变深.故答案为:紫色石蕊试液变红;红色由浅变深;2SO2+O2+2H2O=2H2SO4;(iv)E装置发生SO2+Cl2+2H2O=H2SO4+2HCl,离子反应为:SO2+Cl2+2H2O=4H++SO42﹣+Cl﹣ , 再滴加硝酸钡溶液,观察到生成硫酸钡白色沉淀,离子反应为:SO42﹣+Ba2+=BaSO4↓,故答案为:SO2+Cl2+2H2O=4H++SO42﹣+Cl﹣、SO42﹣+Ba2+=BaSO4↓.
mol/L;(iii)F装置中二氧化硫与水反应生成亚硫酸,溶液显酸性,滴加几滴紫色石蕊试液,观察到的现象是紫色溶液变红,再通入氧气,发生2SO2+O2+2H2O=2H2SO4 , 酸性增强,红色由浅变深.故答案为:紫色石蕊试液变红;红色由浅变深;2SO2+O2+2H2O=2H2SO4;(iv)E装置发生SO2+Cl2+2H2O=H2SO4+2HCl,离子反应为:SO2+Cl2+2H2O=4H++SO42﹣+Cl﹣ , 再滴加硝酸钡溶液,观察到生成硫酸钡白色沉淀,离子反应为:SO42﹣+Ba2+=BaSO4↓,故答案为:SO2+Cl2+2H2O=4H++SO42﹣+Cl﹣、SO42﹣+Ba2+=BaSO4↓.
(i)二氧化硫、二氧化碳的溶解度不大,而二氧化氮水发生氧化还原反应,其溶解度最大;三种气体溶于水得到的溶液均为酸溶液;(ii)①D中二氧化氮、水、氧气反应生成硝酸;②水会充满集气瓶,结合c= ![]() 计算;(iii)F装置中二氧化硫与水反应生成亚硫酸,溶液显酸性,再通入氧气,发生2SO2+O2+2H2O=H2SO4 , 酸性增强;(iv)E装置发生SO2+Cl2+2H2O=H2SO4+2HCl,再滴加硝酸钡溶液,生成硫酸钡沉淀.
计算;(iii)F装置中二氧化硫与水反应生成亚硫酸,溶液显酸性,再通入氧气,发生2SO2+O2+2H2O=H2SO4 , 酸性增强;(iv)E装置发生SO2+Cl2+2H2O=H2SO4+2HCl,再滴加硝酸钡溶液,生成硫酸钡沉淀.

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案