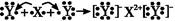题目内容
元素A的阳离子aAm+与元素B的阴离子bBn-具有相同的电子层结构.以下关于A、B元素性 质 的比较中,错误的是:
A.原子序数:A>B B.原子半径:A<B
C.离子半径:aAm+<bBn- D.元素所在的周期数:A>B
A.原子序数:A>B B.原子半径:A<B
C.离子半径:aAm+<bBn- D.元素所在的周期数:A>B
B
试题分析:由题意可知,A的阳离子aAm+与元素B的阴离子bBn-的核外电子数相同,所以满足阴上阳下的原则,元素A在下一周期,元素B在上一周期, A、原子序数A>B,正确;B、原子半径A>B,错误;C、离子半径主要由电子层数、核电荷数决定,前者相同时核电荷数越少半径越大,aAm+<bBn-,正确;D、A所在周期>B所在周期,正确,答案选B。

练习册系列答案
相关题目
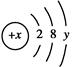 。
。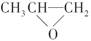 和CO2反应生成可降解聚合物
和CO2反应生成可降解聚合物 ,该反应符合绿色化学的原则
,该反应符合绿色化学的原则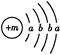 ,X的阳离子与Y的阴离子的电子层结构相同。元素Z、W均为短周期元素,它们原子的最外层电子数均是其电子层数的2倍,Z与Y相邻且Z、W能形成一种WZ2型分子。
,X的阳离子与Y的阴离子的电子层结构相同。元素Z、W均为短周期元素,它们原子的最外层电子数均是其电子层数的2倍,Z与Y相邻且Z、W能形成一种WZ2型分子。
 2Y-+Z↓
2Y-+Z↓