题目内容
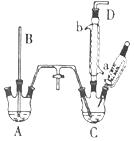
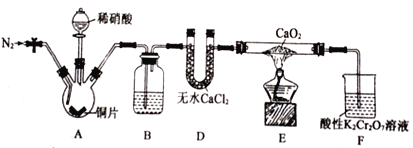
【题目】亚硝酸钙[Ca(NO2)2]是水泥混凝土外加剂的主要原料,某学习小组设计实验制备亚硝酸钙,实验装置如图所示。(夹持装置略去)
已知:2NO+CaO2![]() Ca(NO2)2;2NO2+CaO2
Ca(NO2)2;2NO2+CaO2![]() Ca(NO3)2。
Ca(NO3)2。
Ca(OH)2+NO+NO2=Ca(NO2)2+H2O
请回答下列问题:
(1)向三颈烧瓶中加入稀硝酸之前,应向装置中通入一段时间的N2,原因是______________________。
(2)装置D的名称是__________;装置B中盛装的试剂是___________。
(3)装置F中的酸性K2Cr2O7溶液可将剩余的NO氧化成NO3-,溶液由橙色(Cr2O72-)变为绿色(Cr3+),发生反应的离子方程式为_______________________________。
(4)已知Ca(NO2)2溶液显弱碱性,其对应的酸容易分解,产生NO气体,设计实验证明装置F中有亚硝酸钙生成:_________________________________。
(5)工业上可用石灰乳和硝酸工业的尾气(含NO、NO2)反应,既能净化尾气,又能获得应用广泛的Ca(NO2)2。
①若n(NO)∶n(NO2)>1∶1,则会导致____________________________________;
②若n(NO)∶n(NO2)<1∶1,则会导致____________________________________。
【答案】 排除装置中的空气,防止其将生成的NO氧化为NO2 U型具支干燥管 蒸馏水 Cr2O72-+2NO+6H+=2Cr3++2NO3-+3H2O 取少量E中反应后的固体于试管中,滴加少许稀硫酸,试管口有红棕色气体生成 排放气体中NO含量升高,污染环境 产品中Ca(NO3)2杂质含量升高
【解析】(1)因为NO极易被氧气氧化为NO2,所以实验先通一段时间的氮气的目的是为了将装置内的空气排净,避免将NO氧化。
(2)装置D为U形管,而且两边各有一个支管口,所以是U形具支干燥管。装置B中的试剂就是水,其作用是为了将可能氧化出来的NO2转化为NO。
(3)酸性K2Cr2O7溶液将NO氧化成NO3-, Cr2O72-变为Cr3+,显然在反应物中应该添加氢离子,在生成物中应该添加水,根据化合价升降相等、电荷守恒和原子个数守恒得到方程式为:Cr2O72-+2NO+6H+=2Cr3++2NO3-+3H2O。
(4)已知Ca(NO2)2溶液显弱碱性,说明HNO2是弱酸,其对应的酸(HNO2)容易分解,产生NO气体,所以可以选择向样品中加入强酸,利用强酸制弱酸的原则,生成HNO2,HNO2分解得到NO,NO被空气氧化得到红棕色的NO2,观察现象就能证明NaNO2的存在。
(5)①若n(NO)∶n(NO2)>1∶1,则对于题目给的第三个反应,NO过量,最终排放会污染空气。
②若n(NO)∶n(NO2)<1∶1,则则对于题目给的第三个反应,NO2过量,会发生如下反应:2Ca(OH)2+4NO2=Ca(NO2)2+ Ca(NO3)2+2H2O,所以产物中的硝酸钙杂质的含量会增加。

 暑假作业安徽少年儿童出版社系列答案
暑假作业安徽少年儿童出版社系列答案【题目】在T℃时,Ba(OH)2的稀溶液中c(H+)=10﹣amolL﹣1 , c(OH﹣)=10﹣b molL﹣1 , 已知a+b=12.向该溶液中逐滴加入pH=4的盐酸,测得混合溶液的部分pH如下表所示:
序号 | 氢氧化钡溶液的体积/mL | 盐酸的体积/mL | 溶液的pH |
① | 22.00 | 0.00 | 8 |
② | 22.00 | 18.00 | c |
③ | 22.00 | 22.00 | d |
假设溶液混合前后的体积变化可忽略不计,则下列说法不正确的是( )
A.a=8
B.b=4
C.c=5
D.d=6