题目内容
已知A、B两种气体在一定条件下可发生反应:2A+B=C+3D+4E.现将相对分子质量为M的A气体m g与适量的B充入一个密闭容器内,恰好完全反应且有少量液滴生成,在相同的温度下测得反应前后压强分别为6.06×106 Pa和1.01×107Pa,且测得反应共放热Q kJ.则该反应的热化学方程式是( )
A.2A(g)+B(g)=C(g)+3D(l)+4E(g);△H=+
| ||
B.2A(g)+B(g)=C(l)+3D(g)+4E(g);△H=-
| ||
C.2A(g)+B(g)=C(g)+3D(g)+4E(s);△H=-
| ||
D.2A(g)+B(g)=C(g)+3D(l)+4E(g);△H=-
|
该反应放热,所以△H<0,排除A选项;在密闭容器中气体的压强与其物质的量成正比,即压强之比等于物质的量之比,反应前后压强之比=6.06×106 Pa:1.01×107Pa=3:5,所以反应前后物质的量之比为3:5,物质的量之比等于计量数之比,所以,反应前气体的计量数之和是3,反应后气体的计量数之和是5,显然只有D符合.
故选D.
故选D.

练习册系列答案
相关题目
 kJ/mol
kJ/mol kJ/mol
kJ/mol kJ/mol
kJ/mol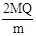 kJ/mol
kJ/mol kJ/mol
kJ/mol kJ/mol
kJ/mol