题目内容
【题目】A、B、C、D、E 都为短周期元素,A 是相对原子质量最小的元素;B 的+1 价阳离子和 C 的—1 价阴离子都与氖原子具有相同的电子层结构;D 在 C 的下一周期,可与 B 形成 BD 型离子化合物;E 和 C 为同一周期元素,其最高价氧化物对应的水化物为一种强酸。请根据以上信息回答下列问题。
(1)B 元素在元素周期表中的位置是第______周期______族。
(2)画出 D 元素的原子结构示意图____________。
(3)与 E 的氢化物分子所含电子总数相等的分子是 ____________(举一例、填化学式,下同 )、离子是____________。
(4)A 与 C 形成的化合物中含有化学键的类型是____________。
(5)D的单质与B的最高价氧化物对应的水化物的溶液发生反应的离子方程式为_________。
【答案】 三 ⅠA 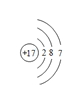 H2O OH- 共价键 Cl2+2OH- =ClO-+Cl-+H2O
H2O OH- 共价键 Cl2+2OH- =ClO-+Cl-+H2O
【解析】(1)B的+1价阳离子与氖原子具有相同的电子层结构,所以B是金属Na,在第三周期第ⅠA族;(2)C的-1价阴离子与氖原子具有相同的电子层结构,所以C是F,D在F的下一周期,可与Na形成BD型离子化合物,即为氯化钠,D为Cl,原子结构示意图为: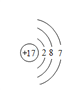 ;(3)E和F为同一周期元素,其最高价氧化物对应的水化物为一种强酸即为硝酸,所以E是N,E的氢化物是氨气,10电子结构,所含电子总数相等的分子有H2O、CH4、HF等,离子有Na+、O2-、OH-、Mg2+、Al3+等;(4)A是相对原子质量最小的元素即为H,H和F形成的是含有共价键的共价化合物;(5)氯气和氢氧化钠反应的离子方程式为:Cl2+2OH-=ClO-+Cl-+H2O。
;(3)E和F为同一周期元素,其最高价氧化物对应的水化物为一种强酸即为硝酸,所以E是N,E的氢化物是氨气,10电子结构,所含电子总数相等的分子有H2O、CH4、HF等,离子有Na+、O2-、OH-、Mg2+、Al3+等;(4)A是相对原子质量最小的元素即为H,H和F形成的是含有共价键的共价化合物;(5)氯气和氢氧化钠反应的离子方程式为:Cl2+2OH-=ClO-+Cl-+H2O。

练习册系列答案
相关题目