题目内容
在18世纪40年代以前,生产硫酸最古老的方法是:以绿矾(FeSO4·7H2O)为原料在蒸馏中煅烧,然后再冷凝至室温,得到一种液体,称之为“绿矾油”。
(1)蒸馏釜所产生的气体中含有的成分是________________________。
(2)绿矾油的成分是________________________。
(3)绿矾油质量分数是________________________。
(4)留在蒸馏釜中的物质是________________________。
(1)蒸馏釜所产生的气体中含有的成分是________________________。
(2)绿矾油的成分是________________________。
(3)绿矾油质量分数是________________________。
(4)留在蒸馏釜中的物质是________________________。
(1)SO2、SO3、H2O (2)H2SO4 (3)绿矾油质量分数=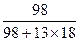 ×100%=29.5% (4)Fe2O3
×100%=29.5% (4)Fe2O3
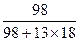 ×100%=29.5% (4)Fe2O3
×100%=29.5% (4)Fe2O3根据题意,写出反应式:
2(FeSO4·7H2O) Fe2O3+SO2+SO3+14H2O
Fe2O3+SO2+SO3+14H2O
2(FeSO4·7H2O)
 Fe2O3+SO2+SO3+14H2O
Fe2O3+SO2+SO3+14H2O
练习册系列答案
 夺冠训练单元期末冲刺100分系列答案
夺冠训练单元期末冲刺100分系列答案 新思维小冠军100分作业本系列答案
新思维小冠军100分作业本系列答案 名师指导一卷通系列答案
名师指导一卷通系列答案
相关题目