题目内容
6.在下列各组物质中,所含原子数相同的是( )| A. | mg O2和mg O3 | B. | 7g N2和标准状况下5.6L CO2 | ||
| C. | 1mol氦气和标准状况下22.4L H2 | D. | 1mol SO2和22.4L H2S |
分析 A.根据n(O)=$\frac{m}{M}$分析;
B.计算出物质的量,根据分子组成计算原子个数;
C.氦气为单原子分子;
D.涉及气体体积应指明温度和压强.
解答 解:A.根据n(O)=$\frac{m}{M}$可知,二者氧原子的物质的量相同,故A正确;
B.7g氮气的物质的量为:$\frac{7g}{28g/mol}$=0.25mol,n(N)=0.5mol,标况下5.6L二氧化碳的物质的量为:$\frac{5.6L}{22.4L/mol}$=0.25mol,含原子数为0.75mol,含有原子数目不相等,故B错误;
C.1mol氦气含1mol氦原子,标准状况下,22.4L氢气的物质的量为1mol,含氢原子2mol,含有原子数目不相等,故C错误;
D.气体体积和温度、压强有关,由于没有指明温度、压强,没法计算22.4L气体的物质的量,故二者含原子数不一定相等,故D错误.
故选A.
点评 本题考查了物质的量的计算,较基础,注意稀有气体为单原子分子.

练习册系列答案
 期末冲刺100分创新金卷完全试卷系列答案
期末冲刺100分创新金卷完全试卷系列答案
相关题目
17.某纯净物由两种原子构成,则该物质( )
| A. | 一定是化合物 | B. | 一定是单质 | ||
| C. | 可能是化合物,也可能是单质 | D. | 一定是同素异形体 |
14.下列离子方程式书写正确的是( )
| A. | 硫化亚铁与盐酸反应:S2-+2H+═H2S↑ | |
| B. | SO2通入溴水中:SO2+Br2+2H2O═SO42-+2Br-+4H+ | |
| C. | 硫酸与氢氧化钡溶液混合:H++SO42-+Ba2++OH-═BaSO4↓+H2O | |
| D. | SO2通入氯化钙溶液中:SO2+Ca2++H2O═CaSO3↓+2H+ |
18.下列关于钠原子和钠离子的叙述正确的是( )
| A. | 钠离子比钠原子少了一个质子 | |
| B. | 钠原子有还原性,钠离子有氧化性 | |
| C. | 钠原子和钠离子有相似的化学性质 | |
| D. | 钠原子不稳定,钠离子稳定,两者具有相同的电子层数 |
15.具有相同质子数的两种粒子( )
| A. | 一定是同种元素 | B. | 一定是一种分子和一种离子 | ||
| C. | 一定是不同离子 | D. | 无法判断 |
16.常温下能在浓HNO3中溶解的金属是( )
| A. | Al | B. | Ag | C. | Fe | D. | Pt |
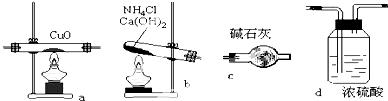 实验室用氨气在加热下还原氧化铜的方法铜的相对原子质量如果选用测定反应物氧化铜和生成物水的质量[m(CO)、m(H2O)]时,如图所示请用下列仪器设计一个简单实验方案.
实验室用氨气在加热下还原氧化铜的方法铜的相对原子质量如果选用测定反应物氧化铜和生成物水的质量[m(CO)、m(H2O)]时,如图所示请用下列仪器设计一个简单实验方案.