题目内容
膦(PH3)又称磷化氢,在常温下是一种无色有大蒜臭味的有毒气体。它的分子构型是
三角锥形。以下关于PH3的叙述正确的是
| A.PH3分子中有未成键的孤对电子 | B.PH3是非极性分子 |
| C.PH3是一种强氧化剂 | D.PH3分子的P-H键是非极性键 |
A
解析试题分析:A.P原子的最外层有5个电子,与三个H原子形成三对共用电子对,达到8个电子的稳定结构。在PH3分子中的P原子上有未成键的孤对电子。正确。B.PH3是由极性键构成的极性分子。错误。C.在PH3中,P的化合价为-3价,在参加反应时容易失去电子,因此该物质是一种强还原剂。D.PH3分子的P-H键是不同种元素的原子形成的共价键,属于极性键。错误。
考点:考查磷化氢的分子结构与性质的知识。

练习册系列答案
相关题目
下列说法或做法错误的是
| A.充满NH3的烧瓶倒置于水中后液面迅速上升,说明NH3易溶于水 |
| B.在胆矾中滴加浓H2SO4,固体变白,说明浓H2SO4具有吸水性 |
| C.将二氧化硫通入品红溶液,溶液褪色,加热后能恢复原色 |
| D.向铜粉中加入浓硫酸,加热,铜粉溶解,同时产生H2 |
在探究新制饱和氯水成分的实验中,下列根据实验现象得出的结论不正确的是
| A.氯水的颜色呈浅绿色,说明氯水中含有Cl2 |
| B.向氯水中滴加硝酸酸化的AgNO3溶液,产生白色沉淀,说明氯水中含有Cl- |
| C.向氯水中加入NaHCO3粉末,有气泡产生,说明氯水中含有H+ |
| D.向FeCl2溶液中滴加氯水,溶液颜色变成棕黄色,说明氯水中含有HClO |
下列说法中正确的是 ( )
| A.6.8 g固体KHSO4与3.9 g固体Na2O2中阴离子数目相同 |
| B.常温下铁、铜均不溶于浓硫酸, 说明常温下铁、铜与浓硫酸均不反应 |
| C.离子化合物中只含离子键 |
| D.中子数为18的氯原子可表示为18Cl |
下列有关说法不正确的是
| A.实验室制取氢气,为了加快反应速率,可向稀H2SO4中滴加少量Cu(NO3)2溶液 |
| B.为处理锅炉水垢中的CaSO4,可先用饱和Na2CO3溶液浸泡,再加入盐酸溶解 |
C.已知NaOH(aq)+HCl(aq)=NaCl(aq)+H2O(l) ΔH=-57.3 kJ·mol-1,则水电离的热化学方程式为:H2O(l) H+(aq)+OH-(aq)ΔH= +57.3 kJ·mol-1 H+(aq)+OH-(aq)ΔH= +57.3 kJ·mol-1 |
| D.生铁发生吸氧腐蚀和析氢腐蚀的负极反应均为:Fe-2e- =Fe2+ |
下列对有关实验事实的解释或得出的结论合理的是
| 选项 | 实验事实 | 解释或结论 |
| A | KI淀粉溶液中滴入氯水变蓝,再通入SO2,溶液褪色 | SO2具有漂白性 |
| B | 将BaSO4浸泡在饱和Na2CO3溶液中,部分BaSO4转化为BaCO3 | Ksp(BaSO4)>Ksp(BaCO3) |
| C | 某钾盐溶于盐酸,产生无色无味气体,该气体通入澄清石灰水,有白色沉淀出现 | 该钾盐可能是K2CO3 |
| D | NaI溶液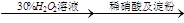 溶液变蓝色 溶液变蓝色 | 酸性条件下H2O2的氧化性比I2强 |
为证明稀硝酸与铜反应产物中气体为NO,设计如图实验(实验过程中活塞2为打开状态),下列说法中不正确的是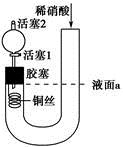
| A.关闭活塞1,加入稀硝酸至液面a处 |
| B.在装置左侧稍加热可以加快稀硝酸与铜的反应速率 |
| C.通过关闭或开启活塞1可以控制反应的进行 |
| D.反应开始后,胶塞下方有无色气体生成,还不能证明该气体为NO |
下列与实验相关的叙述正确的是
| A.稀释浓硫酸时,应将蒸馏水沿玻璃棒缓慢注入浓硫酸中 |
| B.将SO2和Cl2按等物质的量比通入品红溶液中,品红很快褪色 |
| C.NO2与H2O反应的过程中,被氧化的氮原子与被还原的氮原子的个数比为2∶1 |
D.检验某溶液是否含有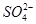 时,应取少量该溶液,依次加入BaCl2溶液和稀盐酸 时,应取少量该溶液,依次加入BaCl2溶液和稀盐酸 |