题目内容
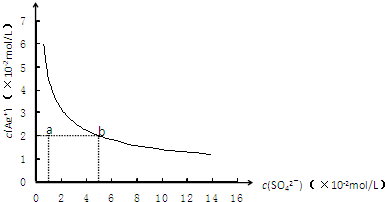
某温度时,Ag2SO4在水溶液中的沉淀溶解平衡曲线如图所示,下列说法中不正确的是

A.b点对应的Ksp等于c点对应的Ksp
B.采取蒸发溶剂的方法可以使溶液从a点变到b点
C.该温度下,Ag2SO4的溶度积常数(Ksp)为1.6×10-5(mol·L-1)3
D.0.02mol·L-1的AgNO3溶液与的0. 2mol·L-1的Na2SO4溶液等体积混合不会生成沉淀
【答案】
B
【解析】
试题分析:溶度积常数只与温度有关系,A正确;B不正确,因为在蒸发过程中,两种离子的浓度都是增加的;根据b点对应的离子浓度可知,该温度下,Ag2SO4的溶度积常数(Ksp)为1.6×10-5(mol·L-1)3, C正确;0.02mol·L-1的AgNO3溶液与的0. 2mol·L-1的Na2SO4溶液等体积混合后Ag+和SO42-浓度分别是0.01mol/L和0.01mol/L,则(0.01)2×0.01=1×10-6<1.6×10-5,因此没有沉淀生成,D正确,答案选B。
考点:考查溶度积常数的有关判断、应用和计算
点评:该题是高考中的常见题型,属于中等难度的试题。主要是考查学生对溶度积常数知识的熟悉掌握程度,以及灵活运用溶度积常数知识解决实际问题的能力。该题综合性强,侧重对学生解题能力的培养和训练,有利于培养学生的逻辑推理能力。

练习册系列答案
 快乐5加2金卷系列答案
快乐5加2金卷系列答案
相关题目
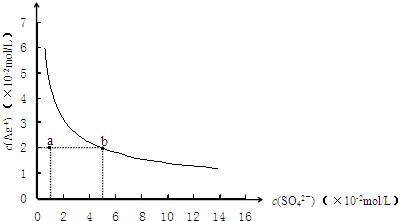

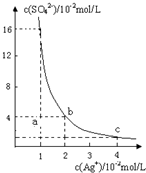 某温度时,Ag2SO4在水溶液中的沉淀溶解平衡曲线如图所示:
某温度时,Ag2SO4在水溶液中的沉淀溶解平衡曲线如图所示: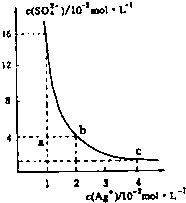 某温度时,Ag2SO4在水溶液中的沉淀溶解平衡曲线如图所示,下列说法中不正确的是( )
某温度时,Ag2SO4在水溶液中的沉淀溶解平衡曲线如图所示,下列说法中不正确的是( )