题目内容
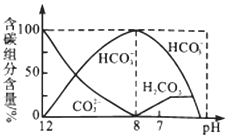
【题目】常温下,向20 mL 0.1 mol/L Na2CO3溶液中逐滴加入0.1 mol/L HCl溶液40 mL,溶液中含碳元素的各种微粒(CO2逸出未画出)的物质的量分数随溶液pH变化的部分情况如图所示,下列说法错误的是
A.在同一溶液中,H2CO3、HCO3-、CO32-不能大量共存
B.已知在25℃,CO32-的水解平衡常数Kh1=2×10-4,当溶液的pH=10时,溶液中c(HCO3-):c(CO32-)=2: 1
C.pH=7时溶液中各种离子其物质的量浓度的大小关系是c(Na+)>c(HCO3-)>c(Cl-)>c(H+)=c(OH-)>c(CO32-)
D.当混合液pH≈6时,开始放出CO2气体
【答案】C
【解析】H2CO3、CO32-反应生成HCO3-,所以H2CO3、HCO3-、CO32-不能大量共存,A正确;CO32-的水解平衡常数Kh1= c(HCO3-)×c(OH-)/ c(CO32-)=2×10-4,已知pH=10时,c(H+)=10-10 mol/L,c(OH-)=10-4 mol/L,因此c(HCO3-)/c(CO32-)=2×10-4/10-4=2,即c(HCO3-):c(CO32-)=2:1,B正确;根据图像可知,pH=8时,溶液为碳酸氢钠和氯化钠(1:1),当pH=7时,部分碳酸氢钠与盐酸反应生成氯化钠和碳酸,因此溶液中c(Na+)>c(Cl-)>c(HCO3-)>c(H+)=c(OH-)>c(CO32-),C错误;由图像可知,当pH≈6时,H2CO3浓度不再增加,说明溶液已饱和,CO2开始逸出,D正确;正确选项C。

 培优口算题卡系列答案
培优口算题卡系列答案 开心口算题卡系列答案
开心口算题卡系列答案 口算题卡河北少年儿童出版社系列答案
口算题卡河北少年儿童出版社系列答案【题目】某研究小组为了探究NaClO溶液的性质,设计了下列实验,并记录实验现象。
实验装置 | 实验序号 | 滴管试剂 | 试管试剂 | 实验现象 |
| ① | 0.2 mol/L NaClO溶液 | 饱和Ag2SO4溶液 | 产生白色沉淀 |
② | CH3COOH溶液 | 光照管壁有无色气泡 | ||
③ | 0.2mol/LFeSO4酸性溶液和KSCN溶液 | 溶液变红 | ||
④ | 0.2mol/L的AlCl3溶液 | 产生白色沉淀 |
则以下判断不正确的是
A. 实验①:发生的反应为Ag++ClO-+H2O=AgCl↓+2OH- B. 实验②:无色气体为O2
C. 实验③:还原性强弱顺序Fe2+>Cl- D. 实验④:ClO-与Al3+的水解相互促进