题目内容
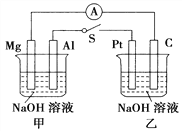
【题目】如图所示,将两烧杯中电极用导线相连,四个电极分别为Mg、Al、Pt、C。当闭合开关S后,以下表述正确的是( )
A. 电流表指针不发生偏转
B. Al、Pt两极有H2产生
C. 甲池pH减小,乙池pH不变
D. Mg、C两极生成的气体在一定条件下可以恰好完全反应
【答案】CD
【解析】A 错 闭合开关S后,甲池是原电池,乙池是电解池,有电流通过,电流表指针偏转
B 甲池中Al和氢氧化钠溶液反应,做负极,Mg电极上有氢气产生。乙池中Pt做阴极,C做阳极,Pt电极有氢气产生
C 甲池氢氧化钠溶液参加了反应,所以,浓度减小,PH减小。乙池电解氢氧化钠溶液,本质是电解水,溶液浓度增大,PH增大。
D Mg极上产生氢气,C极上产生氧气,恰好完全反应,生成水。故选C、D。

 时刻准备着暑假作业原子能出版社系列答案
时刻准备着暑假作业原子能出版社系列答案【题目】某蓄电池反应为NiO2+Fe+2H2O![]() Fe(OH)2+Ni(OH)2。
Fe(OH)2+Ni(OH)2。
(1)该蓄电池充电时,发生还原反应的物质是 (填下列字母),放电时生成Fe(OH)2的质量18 g,则外电路中转移的电子数是 。
A.NiO2 B.Fe C.Fe(OH)2 D.Ni(OH)2
(2)为防止远洋轮船的钢铁船体在海水中发生电化学腐蚀,通常把船体与浸在海水里的Zn块相连,或与该蓄电池这样的直流电源的 极(填“正”或“负”)相连。
(3)以该蓄电池做电源,用右图所示装置,在实验室模拟铝制品表面“钝化”处理的过程中,发现溶液逐渐变浑浊,原因是(用相关的电极反应式和离子方程式表示)。 。

(4)精炼铜时,粗铜应与直流电源的 极(填“正”或“负”)相连,精炼过程中,电解质溶液中c(Fe2+)、c(Zn2+)会逐渐增大而影响进一步电解,甲同学设计如下除杂方案:
![]()
已知:
沉淀物 | Fe(OH)3 | Fe(OH)2 | Cu(OH)2 | Zn(OH)2 |
开始沉淀时的pH | 2.3 | 7.5 | 5.6 | 6.2 |
完全沉淀时的pH | 3.9 | 9.7 | 6.4 | 8.0 |
则加入H2O2的目的是 ,乙同学认为应将方案中的pH调节到8,你认为此观点 (填“正确”或“不正确”),理由是 。
【题目】有五种短周期元素,它们的结构、性质等信息如下表所述:
元素 | 结构、性质等信息 |
A | 是短周期中(除稀有气体外)原子半径最大的元素 |
B | B与A同周期,其最高价氧化物的水化物呈两性 |
C | 元素的气态氢化物极易溶于水,可用作制冷剂 |
D | 是海水中除氢、氧元素外含量最多的元素,其单质或化合物也是自来水生产过程中常用的消毒杀菌剂 |
E | 基态原子的M层全充满,N层没有成对电子,只有一个未成对电子 |
请根据表中信息填写:
⑴A元素在元素周期表中的位置____________________________________________。
⑵离子半径:B_________A(填“大于”或“小于”)。
⑶C原子的电子排布图是______________,其原子核外有________个未成对电子,能量最高的电子为________轨道上的电子,其轨道呈________形。
⑷B的最高价氧化物对应的水化物与A的最高价氧化物对应的水化物反应的离子方程式为_____________,与D最高价氧化物的水化物水溶液反应的化学方程式为___________。
⑸E元素基态原子的电子排布式为____________________.

