题目内容
已知一定温度下,有下列难溶电解质的相关数据
| 物质 | Fe(OH)2 | Cu(OH)2 | Fe(OH)3 |
| KSP/250C | 8.0×10-16 | 2.2×10-20 | 4.0×10-38 |
| 完全沉淀时的pH范围 | ≥9.6 | ≥6.4 | 3~4 |
对含等物质的量的CuSO4、FeSO4、Fe2(SO4)3的混合溶液的说法,不正确的是
A.向该混合溶液中加过量铁粉,能观察到红色固体析出
B.向该混合溶液中逐滴加入NaOH溶液,最先看到红褐色沉淀
C.该混合溶液中c(SO42-):[c(Cu2+)+ c(Fe2+)+ c(Fe3+)]>5∶4
D.向该混合溶液中加入适量氯水,并调pH至3~4后过滤,能得到纯净的CuSO4溶液
D
解析试题分析:A.发生反应:Fe2(SO4)3+Fe=3FeSO4; CuSO4+Fe=FeSO4+Cu.因此能观察到红色固体析出。正确。B.由于该溶液显酸性,而形成沉淀需要的pH最小的是Fe(OH)3。因此向该混合溶液中逐滴加入NaOH溶液,最先看到是产生Fe(OH)3红褐色沉淀。正确。C.假设各种物质的物质的量都是1mol.由于在同一溶液中,离子的浓度比即是离子的物质的量的比。所以若盐不发生水解反应,则该混合溶液中c(SO42-):[c(Cu2+)+ c(Fe2+)+ c(Fe3+)]=(1+1+3):(1+1+2)=5∶4.但是由于这几种盐都是强酸弱碱盐,金属阳离子会发生水解反应,会消耗。因此二者的比值大于5∶4。正确。D.向该混合溶液中加入适量氯水,会发生氧化还原反应:2Fe2++Cl2=2Fe3++2Cl-.并调pH至3~4后会形成Fe(OH)3红褐色沉淀。过滤,得到溶液含有CuSO4和CuCl2.错误。
考点:考查混合溶液中加入物质时反应的先后顺序及实验现象的知识。

 小学教材全测系列答案
小学教材全测系列答案下列溶液中,微粒浓度关系正确的是( )
| A.含有 NH4+、Cl-、H+、OH-的溶液中,其离子浓度可能是c(Cl-)> c(NH4+)>c(OH-)>c(H+) |
| B.常温下pH=6的醋酸与醋酸钠的混合溶液中c(Na+)>c(CH3COO-) |
| C.0.1 mol·L-1的Na2S溶液中,c(OH-)=c(H+)+c(HS-)+2c(H2S) |
| D.常温下pH=3的一元酸和pH=11的一元碱等体积混合后的溶液中一定是c(OH-)=c(H+) |
将0.1 mol/L的NH3·H2O溶液加水稀释,下列说法正确的是( )
| A.c(NH)/c(NH3·H2O)比值减小 | B.OH-个数将减少 |
| C.c(OH-)/c(NH3·H2O)比值减小 | D.NH4+浓度将减小 |
实验室用标准盐酸溶液测定某NaOH溶液的浓度,用甲基橙作指示剂,下列操作中可能使测定结果偏高的是( )
| A.酸式滴定管在装酸液前用标准盐酸溶液润洗2~3次 |
| B.开始实验时酸式滴定管尖嘴部分有气泡,在滴定过程中气泡消失 |
| C.锥形瓶内溶液颜色变化由黄色变橙色,立即记下滴定管液面所在刻度 |
| D.盛NaOH溶液的锥形瓶滴定前用NaOH溶液润洗2~3次 |
向10 mL 0.1 mol·L-1Na2CO3溶液中逐滴滴加V mL 0.1 mol·L-1HCl溶液,下列有关滴定过程中粒子浓度关系正确的是
A.当V=0时,c(OH-)=c(H+)+c(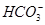 )+c(H2CO3) )+c(H2CO3) |
B.当V=5时,c(Na+)+c(H+)=2c( )+c( )+c(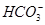 )+c(OH-) )+c(OH-) |
C.当V=10时,c(Cl-)=c( )+c( )+c(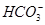 )+c(H2CO3) )+c(H2CO3) |
D.当V=15时,c(Na+)=c(Cl-)>c(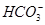 )>c(OH-)>c(H+) )>c(OH-)>c(H+) |
下列有关电解质溶液的说法正确的是
| A.在蒸馏水中滴加浓H2SO4,Kw不变 |
B.CH3COOH溶液加水稀释后,溶液中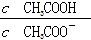 的值减小 的值减小 |
C.Na2CO3溶液中加入少量Ca(OH)2固体, 水解程度减小,溶液的pH减小 水解程度减小,溶液的pH减小 |
| D.NaCl溶液和CH3COONH4溶液均显中性,两溶液中水的电离程度相同 |
一定温度下的难溶电解质AmBn在水溶液中达到溶解平衡时。已知下表数据
| 物质 | Fe(OH)2 | Cu(OH)2 | Fe(OH)3 |
| Ksp(25 ℃) | 8.0×10-16 | 2.2×10-20 | 4.0×10-38 |
| 完全沉淀时的pH值 | ≥9.6 | ≥6.4 | 3~4 |
对含等物质的量的CuSO4、FeSO4、Fe2(SO4)3的混合溶液的说法,不科学的是
A.向该溶液中加少量铁粉不能观察到红色固体析出
B.该溶液中c(SO):[c(Cu2+)+c(Fe2+)+c(Fe3+)]>5∶4
C.向该混合溶液中逐滴加入NaOH溶液,最先看到红褐色沉淀
D.向该溶液中加入适量氯水,并调节pH值到3~4后过滤,得到纯净的CuSO4溶液
关于10 mL 0.1 mol·L-1的NH3·H2O溶液,下列说法正确的是
| A.25 ℃时,若溶液的pH=11,则Kb(NH3·H2O)=1×10-6 mol·L-1 |
B.向溶液中加入少量CH3COONa固体,溶液中的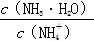 值变小 值变小 |
C.向溶液中加入10 mL 0.1 mol·L-1 HCl,所得溶液中离子浓度大小顺序为c(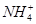 )>c(Cl-)>c(H+)>c(OH-) )>c(Cl-)>c(H+)>c(OH-) |
D.向溶液中加入5 mL 0.1 mol·L-1 HCl,所得溶液中离子的浓度一定符合:c(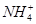 )+c(H+)=c(Cl-)+c(OH-) )+c(H+)=c(Cl-)+c(OH-) |
下列关于溶液的酸碱性,说法正确的是( )
| A.pH=7的溶液是中性 |
| B.中性溶液中一定:c(H+)=1.0×10-7 mol·L-1 |
| C.c(H+)=c(OH-)的溶液呈中性 |
| D.在100°C时,纯水的pH<7,因此显酸性 |