��Ŀ����
����Ŀ����֪AΪ����ɫ���壬T��RΪ���ֳ�������;�ܹ�Ľ������ʣ�D�Ǿ��д��Եĺ�ɫ���壬C����ɫ��ζ�����壬H�ǰ�ɫ���������ڳ�ʪ������Ѹ�ٱ�Ϊ����ɫ�����ձ�Ϊ���ɫ���塣
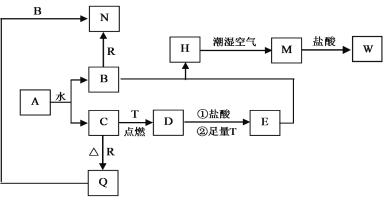
��1��д���������ʵĻ�ѧʽ��A��_______��D��_________��R��____________��
��2����Ҫ��д���з�Ӧ����ʽ��
H�ڳ�ʪ�����б��M�Ĺ����еĻ�ѧ����ʽ____________________��
B��R��Ӧ����N�����ӷ���ʽ________________________________��
D�����ᷴӦ�����ӷ���ʽ_____________________________________��
��3����������C�ķ���_________________________________________��
���𰸡�Na2O2 Fe3O4 Al 4Fe(OH)2+O2+2H2O��4Fe(OH)3 2Al+2OH��+2H2O��2AlO2��+3H2�� Fe3O4+8H+��Fe2++2Fe3++4H2O �ô����ǵ�ľ�������Թܿڣ��������ǵ�ľ����ȼ��˵������������
��������
����AΪ����ɫ���壬���ܺ�ˮ��Ӧ����AΪNa2O2��A��ˮ��Ӧ����NaOH��O2��C����ɫ��ζ�����壬��C��O2��B��NaOH��D�Ǿ��д��Եĺ�ɫ���壬��D��Fe3O4��Fe��������ȼ��������������������T��Fe��R��������Ӧ����������Q��Q�ܺ�NaOH��Һ��Ӧ����Q��Al2O3��R��Al��N��NaAlO2��H�ǰ�ɫ���������ڳ�ʪ������Ѹ�ٱ�Ϊ����ɫ�����ձ�Ϊ���ɫ����M����H��Fe(OH)2��M��Fe(OH)3��Fe3O4��HCl��Fe��Ӧ��õ�E��EΪFeCl2��Fe(OH)3��HCl��Ӧ����W����W��FeCl3��

����Ŀ��������X����ͨ��Y��Һ�У�ʵ������Ԥ�������һ�µ������
X���� | Y��Һ | Ԥ������� |
| |
�� | CO2 | ����Na2CO3��Һ | ��ɫ�������� | |
�� | SO2 | Ba(NO3)2��Һ | ��ɫ�������� | |
�� | Cl2 | AgNO3��Һ | ��ɫ�������� | |
�� | NH3 | AlCl3��Һ | ��ɫ�������� |
A. ֻ�Т٢ڢ� B. ֻ�Т٢ڢ� C. ֻ�Т٢ۢ� D. �٢ڢۢ�