题目内容
(15分)填写下列空白:
(1)Fe(OH)3胶体呈红褐色,插入两个惰性电极,通直流电一段时间,阴极附近的颜色逐渐变深,这种现象叫______________。
(2)强光通过Fe(OH)3胶体,可看到光带,这种现象叫________________。
(3)淀粉与食盐的混合液放在肠衣(半透膜)中,并把它悬挂在盛有蒸馏水的烧瓶里,从而使淀粉与食盐分离,这种方法_______________。
(4)Fe(OH)3胶体加硅酸胶体,胶体变得浑浊,这是发生了____________。
(5)已知冰的熔化热为6.0 kJ/mol,冰中氢键键能为20 kJ/mol,假设1 mol冰中有2 mol 氢键,且熔化热完全用于破坏冰的氢键,则最多只能破坏冰中_____%的氢键
(1)Fe(OH)3胶体呈红褐色,插入两个惰性电极,通直流电一段时间,阴极附近的颜色逐渐变深,这种现象叫______________。
(2)强光通过Fe(OH)3胶体,可看到光带,这种现象叫________________。
(3)淀粉与食盐的混合液放在肠衣(半透膜)中,并把它悬挂在盛有蒸馏水的烧瓶里,从而使淀粉与食盐分离,这种方法_______________。
(4)Fe(OH)3胶体加硅酸胶体,胶体变得浑浊,这是发生了____________。
(5)已知冰的熔化热为6.0 kJ/mol,冰中氢键键能为20 kJ/mol,假设1 mol冰中有2 mol 氢键,且熔化热完全用于破坏冰的氢键,则最多只能破坏冰中_____%的氢键
(1)电泳 (2)丁达尔效应 (3)渗析 (4)胶体的凝聚 (5)15%
略

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目

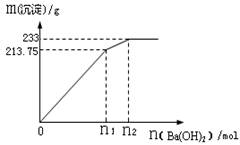
 水的产物),试用有关的电极反应式,离子方程式和化学方程式表示Fe(OH)3的生成:
水的产物),试用有关的电极反应式,离子方程式和化学方程式表示Fe(OH)3的生成: ;
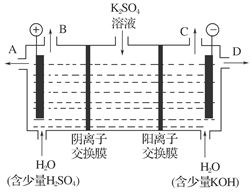
;

 红棕色物质
红棕色物质 4e-→4OH-
4e-→4OH-