题目内容
20.二氯化二硫(S2Cl2)可用作橡胶工业的硫化剂,常温下它是橙黄色有恶臭的液体,它的分子结构与H2O相似,熔点为193K,沸点为411K,遇水很容易反应,产生的气体能使品红褪色,S2Cl2可由干燥的氯气通入熔融的硫中制得.下列有关说法正确的是( )| A. | S2Cl2晶体中存在离子键和极性共价键 | |
| B. | S2Cl2分子中各原子均达到8电子稳定结构 | |
| C. | S2Cl2的水溶液能导电,所以S2Cl2是电解质 | |
| D. | S2Cl2与水反应后生成的气体通入石蕊试液中,现象是溶液先变红后褪色 |
分析 A.分子结构与H2O相似,为分子晶体;
B.结构为Cl-S-S-Cl,Cl、S均满足最外层8电子;
C.遇水很容易反应,S2Cl2本身不能发生电离;
D.产生的气体能使品红褪色,可知生成二氧化硫,还生成S、HCl,二氧化硫为酸性氧化物.
解答 解:A.分子结构与H2O相似,为分子晶体,不含离子键,故A错误;
B.Cl最外层有7个电子、S最外层有6个电子,由结构为Cl-S-S-Cl可知,Cl、S均满足最外层8电子稳定结构,故B正确;
C.遇水很容易反应,S2Cl2本身不能发生电离,为非电解质,故C错误;
D.产生的气体能使品红褪色,可知生成二氧化硫,二氧化硫为酸性氧化物,则气体通入石蕊试液中,现象是溶液变红,故D错误;
故选B.
点评 本题考查物质结构与性质,为高频考点,把握化学键、分子结构、物质的性质、电解质判断为解答的关键,侧重分析与应用能力的考查,综合性较强,题目难度不大.

练习册系列答案
 小学同步三练核心密卷系列答案
小学同步三练核心密卷系列答案
相关题目
10.amL三种气态烃的混合物与足量氧气混合点燃爆炸后,恢复到原来的状态(常温常压),体积共缩小2amL.则三种烃可能是( )
| A. | CH4 C2H4 C3H4 | B. | C2H6 C3H6 C4H6 | ||
| C. | CH4 C2H6 C3H8 | D. | C2H4 C2H2 CH4 |
15.取一定量的镁铝合金均分为两份,分别与足量的盐酸、NaOH溶液充分反应,产生气体的物质的量之比为5:3.合金与NaOH溶液反应的化学方程式为2Al+2NaOH+2H2O=2NaAlO2+3H2↑.
17.已知: ,由于醚键比较稳定故利用 此反应可保护醛基,也可以合成缩醛类有机物,下列说法中不正确的是( )
,由于醚键比较稳定故利用 此反应可保护醛基,也可以合成缩醛类有机物,下列说法中不正确的是( )
 ,由于醚键比较稳定故利用 此反应可保护醛基,也可以合成缩醛类有机物,下列说法中不正确的是( )
,由于醚键比较稳定故利用 此反应可保护醛基,也可以合成缩醛类有机物,下列说法中不正确的是( )| A. | 保护 1mol 醛基时也可用2molCH3CH2OH | |
| B. | 合成 1mol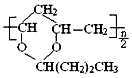 需要 1mol 需要 1mol 和 nmolCH3CH2CH2CHO 和 nmolCH3CH2CH2CHO | |
| C. | 通过上述反应合成的 其核磁共振氢谱中峰面积之比为1:1:1:1:1:2:2:3 其核磁共振氢谱中峰面积之比为1:1:1:1:1:2:2:3 | |
| D. | 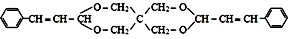 可由 C(CH2OH)4 与 可由 C(CH2OH)4 与 通过上述反应得到 通过上述反应得到 |
18. 有机物A、B均为合成某种抗支气管哮喘药物的中间体,如图所示,A在一定条件下可转化为B,下列说法错误的是( )
有机物A、B均为合成某种抗支气管哮喘药物的中间体,如图所示,A在一定条件下可转化为B,下列说法错误的是( )
 有机物A、B均为合成某种抗支气管哮喘药物的中间体,如图所示,A在一定条件下可转化为B,下列说法错误的是( )
有机物A、B均为合成某种抗支气管哮喘药物的中间体,如图所示,A在一定条件下可转化为B,下列说法错误的是( )| A. | 分子B中只含有3种官能团 | |
| B. | 分子A中所有碳原子不可能位于同一平面 | |
| C. | 分子B能发生银镜反应,但不能发生水解反应 | |
| D. | 用FeCl3溶液可检验物质B中是否混有A |
 .
.