题目内容
【题目】工业利用含有Al2O3、SiO2和少量FeOxFe2O3的铝灰制备硫酸铝晶体与三草酸合铁酸钾[K2Fe(C2O4)33H2O]在的流程如图所示: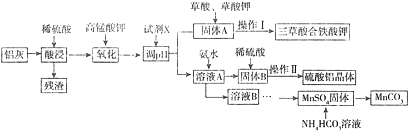
已知:生成氢氧化物的pH
Al(OH)3 | Fe(OH)3 | |
开始沉淀时 | 3.6 | 2.1 |
完全沉淀时 | 5.2 | 3.2 |
回答下列问题:
(1)为提高酸浸速率,应采用的措施是(答出两条) , 残渣的主要成分是;
(2)写出氧化过程中反应的了新方程式;
(3)试剂X的化学式是 , pH的调控范围是;
(4)操作Ⅱ的晶体步骤为 , 过滤洗涤、低温干燥,若操作Ⅰ与操作Ⅱ相同,则洗涤三草酸合铁酸钾以获得干燥晶体的试剂最好是;a.先热水后酒精 b.先冷水后酒精 c.先酒精后热水 d.先酒精后冷水
(5)生成MnCO3沉淀的离子方程式为 .
【答案】
(1)适当提高硫酸的浓度、加热、搅拌;SiO2
(2)MnO4﹣+5Fe2++8H+=Mn2++5Fe3++4H2O
(3)Al2O3或Al(OH)3;3.2≤pH<3.6
(4)蒸发浓缩、降温结晶;b
(5)Mn2++2HCO3﹣=MnCO3↓+H2O+CO2↑
【解析】解:铝灰(含Al、Al2O3及少量SiO2和FeOxFe2O3),加入过量稀硫酸酸溶过滤,滤液为硫酸铝、硫酸亚铁、硫酸铁,残渣为二氧化硅和不溶性杂质,过滤后在滤液中加入稍过量高锰酸钾溶液氧化亚铁离子为铁离子,用氧化铝或氢氧化铝调节溶液PH使铁离子全部沉淀,铝离子不沉淀,得固体A为氢氧化铁,溶液A中含有铝离子,溶液A中加入氨水后得固体B为氢氧化铝,固体B中加入稀硫酸得硫酸铝溶液,再将硫酸铝溶液蒸发浓缩、降温结晶过滤洗涤得到硫酸铝钾晶体,溶液B中含有锰离子和硫酸根离子,硫酸锰固体溶于碳酸氢铵溶液可得碳酸锰沉淀,(1)为提高酸浸速率,可以适当提高硫酸的浓度、加热、搅拌等,根据上面的分析可知,残渣的主要成分是SiO2 , 所以答案是:适当提高硫酸的浓度、加热、搅拌;SiO2;(2)图中氧化过程就是高锰酸钾将亚铁离子氧化为铁离子,反应的离子方程式为MnO4﹣+5Fe2++8H+=Mn2++5Fe3++4H2O,所以答案是:MnO4﹣+5Fe2++8H+=Mn2++5Fe3++4H2O;(3)根据上面的分析可知,试剂X的化学式是Al2O3或Al(OH)3 , 要使铁离子完全沉淀且铝离子不能沉淀,所以pH的调控范围是3.2≤pH<3.6,所以答案是:Al2O3或Al(OH)3;3.2≤pH<3.6;(4)操作Ⅱ就是从硫酸铝溶液中得到硫酸铝晶体,步骤为 蒸发浓缩、降温结晶、过滤洗涤、低温干燥,若操作Ⅰ与操作Ⅱ相同,则洗涤三草酸合铁酸钾以获得干燥晶体的试剂最好是先冷水后酒精,这样即可以除去可溶性杂质,又可以减小三草酸合铁酸钾的溶解,又便于干燥,故选b,
所以答案是:蒸发浓缩、降温结晶;b;(5)生成MnCO3沉淀的离子方程式为Mn2++2HCO3﹣=MnCO3↓+H2O+CO2↑,所以答案是:Mn2++2HCO3﹣=MnCO3↓+H2O+CO2↑.

【题目】硫酸的年产量高低常用于衡量一个国家化工生产水平的高低.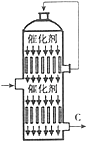
(1)以黄铁矿为原料生产SO2时反应的化学方程式为: , 该反应在中进行(填设备名称);
(2)某科研小组测得某硫酸工厂生产工厂中SO2的平衡转化率与外部条件的关系如下表所示,则生产过程中,最适合的生产条件是;
压强(Pa) | 1.013×105 | 5.065×105 | 10.13×105 | 15.195×105 |
400 | 99.61% | 99.72% | 99.84% | 99.88×105 |
500 | 96.75% | 97.67% | 98.52% | 98.94% |
600 | 85.20% | 88.97% | 92.76% | 94.68% |
(3)接触室内有一热交换器,其作用是 , 若将从C处(如图)出来的气体通入BaCl2溶液中,则主要负电离子方程式为(写总反应式);
(4)下列做法中,与提高硫酸工业的经济效益无关的是;a.适当地对黄铁矿进行粉碎
b.在接触室中使用适当过量的O2
c.利用生产中的余热发电或供暖
d.对废水进行无害化处理后再排放
(5)硫酸工业会产生许多对环境有害的物质,因此无论是工厂厂址的选择还是生产过程中有害成分的处理都要充分考虑环保的要求;①某市计划建一个硫酸工厂,厂址有A、B、C三个地方可供选择,假设最终该厂建在B地,你认为选择B地建厂的理由是(至少回答两点)、;
②将尾气中SO2在一定条件下转化为CaSO4 , 然后利用焦炭将其转化为CaS(另有一种可燃性气体生成)具有重要的意义,写出CaSO4转化为CaS的化学方程式;
(6)若用等质量的硫磺,FeS2生产硫酸,假设原料的总利用率均为90%,则二者得到的硫酸质量比为 .