题目内容
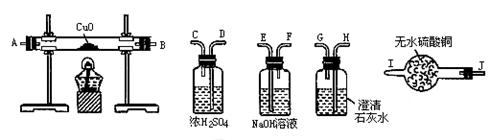
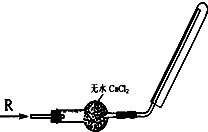
某学生要用50 mL NaOH溶液和CO2来制取纯Na2CO3溶液,已知CO2气体在通入NaOH溶液过程中极易生成NaHCO3,且无明显现象。
实验室有下列试剂:①未知浓度的NaOH溶液 ②37%的盐酸 ③37%的硫酸 ④14%的盐酸 ⑤大理石⑥饱和NaHCO3溶液
实验室有下列仪器:量筒,烧杯,橡皮管,玻璃导管,分液漏斗,烧杯,洗气瓶,酒精灯。
已知下表中各物质在常温时的溶解度(g/100 g H2O)
小题1:本实验除了下面图给的仪器外,还应有: (仪器安装补完整)。
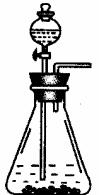
小题2:实验为保证制得Na2CO3的纯度,应选用的药品,除①外,还应需要: 。
小题3:简要叙述实验步骤,直到制得纯碳酸钠溶液 。
小题4:根据给出的溶解度表,若保证在配制过程中不会有晶体析出,所用氢氧化钠溶液中含NaOH的质量分数的最大值是多少(写出计算步骤和必要的文字说明)?
实验室有下列试剂:①未知浓度的NaOH溶液 ②37%的盐酸 ③37%的硫酸 ④14%的盐酸 ⑤大理石⑥饱和NaHCO3溶液
实验室有下列仪器:量筒,烧杯,橡皮管,玻璃导管,分液漏斗,烧杯,洗气瓶,酒精灯。
已知下表中各物质在常温时的溶解度(g/100 g H2O)
| Na2CO3 | NaHCO3 | NaCl | Na2SO4 | NaHSO4 | NaOH |
| 15.9 | 8.4 | 35 | 35.5 | 20 | 40 |

小题2:实验为保证制得Na2CO3的纯度,应选用的药品,除①外,还应需要: 。
小题3:简要叙述实验步骤,直到制得纯碳酸钠溶液 。
小题4:根据给出的溶解度表,若保证在配制过程中不会有晶体析出,所用氢氧化钠溶液中含NaOH的质量分数的最大值是多少(写出计算步骤和必要的文字说明)?
小题1:洗气瓶,烧杯,量筒;装置如下图所示:
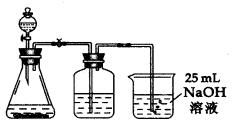
小题2:④⑤⑥
小题3:①取25 mL NaOH溶液通入过量的CO2气体,至CO2不再溶解;
②小心煮沸溶液1~2分钟,排出溶液中溶解的CO2气体;
③在得到的溶液中加入另一半(25 mL)NaOH溶液,使溶液充分混合即得纯的碳酸钠。
小题4:要保证在配制过程中不会有晶体析出,即100 g水中最多溶解8.4 g NaHCO3,根据化学方程式:NaOH+CO2=NaHCO3,生成8.4 g NaHCO3需NaOH固体4 g,NaOH溶液的质量分数最大只能为
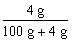 =3.85%,所以配制过程中不会有晶体析出,就必须使NaOH溶液的质量分数≤3.85%。
=3.85%,所以配制过程中不会有晶体析出,就必须使NaOH溶液的质量分数≤3.85%。本题要求制得纯净的碳酸钠,根据题意不能在氢氧化钠中直接通二氧化碳来制纯净Na2CO3,否则不纯,因为这样二氧化碳的量很难控制,若CO2生成碳酸氢钠,若CO2不足则氢氧化钠反应不完全。所以只有把氢氧化钠分成两等份,其中一份通足量的二氧化碳使其完全生成碳酸氢钠后,再把另一份加入其中让其完全转化为碳酸钠。在制CO2时应选用较稀的盐酸,便于控制反应速率和减少HCl的干扰。

练习册系列答案
 七星图书口算速算天天练系列答案
七星图书口算速算天天练系列答案
相关题目
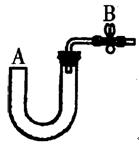
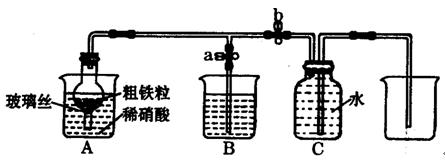
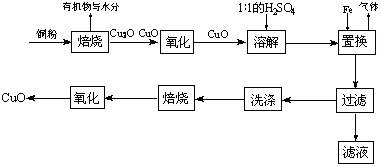
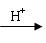 Cu+Cu2+)。请你设计一个简单的实验检验焙烧后固体(假设只含铜的氧化物)中是否含有Cu2O。
Cu+Cu2+)。请你设计一个简单的实验检验焙烧后固体(假设只含铜的氧化物)中是否含有Cu2O。 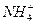 、
、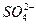 、Fe2+和结晶水,设计了下列操作步骤:①取少量该化合物加热,发现试管口处有液体,该液体能使无水硫酸铜变蓝;②另取少量该化合物溶于水中,滴加少量的氯水,再加入KSCN溶液,有血红色出现;③取少量溶液于试管中,加入盐酸,没有现象,再加入BaCl2溶液,有白色沉淀生成;④取少量溶液于试管中,加入浓的NaOH溶液,微热有使湿润的红色石蕊试纸变蓝的气体产生,同时也有白色沉淀产生,该沉淀很快变成灰绿色沉淀。
、Fe2+和结晶水,设计了下列操作步骤:①取少量该化合物加热,发现试管口处有液体,该液体能使无水硫酸铜变蓝;②另取少量该化合物溶于水中,滴加少量的氯水,再加入KSCN溶液,有血红色出现;③取少量溶液于试管中,加入盐酸,没有现象,再加入BaCl2溶液,有白色沉淀生成;④取少量溶液于试管中,加入浓的NaOH溶液,微热有使湿润的红色石蕊试纸变蓝的气体产生,同时也有白色沉淀产生,该沉淀很快变成灰绿色沉淀。