题目内容
【题目】称取(NH4)2SO4和NH4HSO4混合物样品7.24g,加入含0.1molNaOH的溶液,完全反应,生成NH3 1792ml(标准状况),则(NH4)2SO4和NH4HSO4的物质的量比为( )
A.1:1
B.1:2
C.1.87:1
D.3.65:1
【答案】C
【解析】解:假设混合物完全为(NH4)2SO4时消耗NaOH的量最小,7.24g(NH4)2SO4的物质的量为: ![]() ≈0.0548mol,消耗氢氧化钠的物质的量为0.0548mol×2=0.1096mol>0.1mol,说明氢氧化钠的物质的量不足, (NH4)2SO4和NH4HSO4混合物样品中加入氢氧化钠溶液后,先与反应NH4HSO4 , 然后与(NH4)2SO4反应生成氨气,标准状况下生成氨气的物质的量为:
≈0.0548mol,消耗氢氧化钠的物质的量为0.0548mol×2=0.1096mol>0.1mol,说明氢氧化钠的物质的量不足, (NH4)2SO4和NH4HSO4混合物样品中加入氢氧化钠溶液后,先与反应NH4HSO4 , 然后与(NH4)2SO4反应生成氨气,标准状况下生成氨气的物质的量为: ![]() =0.08mol,
=0.08mol,
则与氢离子反应消耗NaOH的物质的量为:0.1mol﹣0.08mol=0.02mol,故NH4HSO4的物质的量为0.02mol,
所以(NH4)2SO4的质量为:7.24g﹣115g/mol×0.02mol=4.94g,其物质的量为: ![]() ≈0.0374mol,
≈0.0374mol,
则NH4)2SO4和NH4HSO4的物质的量比为:0.0375mol:0.02mol=1.87:1,
故选C.

练习册系列答案
相关题目
【题目】下列实验方案中不能达到相应实验目的是( )
A | B | C | D | |
方案 |
|
|
|
|
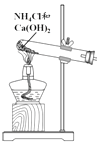
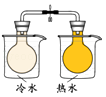
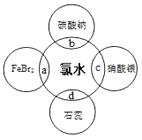
目的 | 探究浓度对化学反应速率的影响 | 制备氨气 | 室温下比较NaHCO3和Na2CO3的溶解度 | 探究温度对化学平衡的影响 |
A.A
B.B
C.C
D.D