题目内容
17.聚合氯化铝(PAC)的化学式为[Al2(OH)nCl6-n]m,是一种无机高分子混凝剂.制备时涉及如下反应:Al(OH)3与[Al(OH)2(H2O)4]Cl反应生成H2O和Al2(OH)nCl6-n,则该反应中两种反应物的计量数之比为( )| A. | 1﹕1 | B. | 1﹕m | C. | (n-4)﹕(6-n) | D. | (4-n)﹕(6-n) |
分析 反应前后同种元素元素数目不变,假设Al2(OH)nCl6-n的化学计量数为1,根据原子守恒进行解答.
解答 解:假设Al2(OH)nCl6-n的化学计量数为1,
根据Cl原子守恒,可知[Al(OH)2(H2O)4]Cl的化学计量数为(6-n),
根据Al原子守恒,可知Al(OH)3的化学计量数为2-(6-n)=(n-4),
故[Al(OH)2(H2O)4]Cl的化学计量数之比为(n-4):(6-n),
故选:C.
点评 本题考查化学方程式有关计算,比较基础,侧重对原子守恒的考查.

练习册系列答案
 黎明文化寒假作业系列答案
黎明文化寒假作业系列答案
相关题目
7.已知热化学方程式:SO2(g)+$\frac{1}{2}$O2(g)?SO3(g)△H=-98.32kJ/mol,在容器中充入4mol SO2和1mol O2充分反应,最终放出的热量为( )
| A. | =393.28 kJ | B. | =196.64 kJ | C. | <196.64 kJ | D. | >196.64 kJ |
8.某植物营养液含有0.2molK+、0.25molZn2+、0.4molCl-和SO42-,则SO42-的物质的量为( )
| A. | 0.1mol | B. | 0.15mol | C. | 0.3mol | D. | 0.5mol |
2.某物质A加热时按下式分解:2A═2B+C+3D (产物均为气体),现测得由生成物组成的混合物气体对H2的相对密度为22.86.则反应物A的摩尔质量为( )
| A. | 22.86g•mol-1 | B. | 45.72g•mol-1 | C. | 80.01g•mol-1 | D. | 137.2g•mol-1 |
7.在一定温度下,向容积为1L的密闭容器中加入1mol A气体和2mol B气体,发生反应:A(g)+2B(g)?2C(g),下列情况能说明该反应达到平衡状态的是( )
| A. | 容器内A、B、C的浓度之比为1:2:2 | |
| B. | 单位时间消耗0.1 mol•L-1 A,同时消耗0.2 mol•L-1 B | |
| C. | 容器内压强不随时间变化 | |
| D. | 容器内平均相对分子质量不随时间变化 |
 X、Y、Z、Q、W、N核电荷数依次增大的六种元素中,Y原子核外的L层电子数是K层的两倍,Q原子核外的L层中只有两个未成对电子,X与Y、Q可以以原子个数2:1或1:1形成化合物.W与Q同主族,元素N的第三能层共有5对成对电子.请回答下列问题:
X、Y、Z、Q、W、N核电荷数依次增大的六种元素中,Y原子核外的L层电子数是K层的两倍,Q原子核外的L层中只有两个未成对电子,X与Y、Q可以以原子个数2:1或1:1形成化合物.W与Q同主族,元素N的第三能层共有5对成对电子.请回答下列问题: ;
;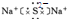 .
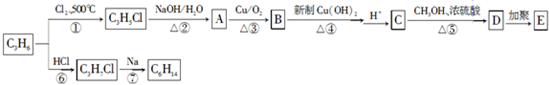
. 
 .
. +6NaBr.
+6NaBr.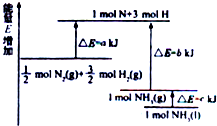 氮及其化合物与科技、生活等密切相关.
氮及其化合物与科技、生活等密切相关.