题目内容
1.某混合气体由一种气态烷烃和一种气态烯烃组成,在同温同压下,混合气体对氢气的相对密度为13,在标况下,将44.8L混合气体通入足量溴水,溴水质量增重28.0g,剩余气体1.5mol.通过计算回答:(1)混合气体中气态烷烃的化学式:CH4
(2)混合气体中两种气体的物质的量之比:n(烷烃):n(烯烃)═3:1
(3)写出混合气体中气态烯烃可能的结构简式:CH2=CH-CH2CH3,CH3-CH=CH-CH3,CH2=C(CH3)2(有多少种填多少种).
分析 (1)相同条件下,密度之比等于相对分子质量之比,据此计算混合气体的相对分子质量,进而确定含有的烷烃;
(2)根据n=$\frac{V}{Vm}$计算44.8L混合气体的物质的量,再根据m=nM计算混合气体的质量,溴水质量增重28g为烯烃的质量,进而计算烷烃的质量与物质的量,再计算烯烃的物质的量,据此解答;
(3)由烯烃的质量与物质的量,根据M=$\frac{m}{n}$计算其摩尔质量,据此计算烯烃的分子式,书写可能的结构.
解答 解:(1)在同温同压下,混合气体对氢气的相对密度为13,故混合气体的平均相对分子质量为13×2=26,故一定含有甲烷,
故答案为:CH4;
(2)标况下44.8L混合气体的物质的量为$\frac{44.8L}{22.4L/mol}$=2mol,故混合气体的总质量为2mol×26g/mol=52g,溴水质量增重28g为烯烃的质量,故甲烷的质量为52g-28g=24g,故甲烷的物质的量为$\frac{24g}{16g/mol}$=1.5mol烯烃的物质的量为2mol-1.5mol=0.5mol,故n(CH4):n(烯烃)=1.5mol:0.5mol=3:1,
故答案为:n(CH4):n(烯烃)=3:1;
(3)烯烃的摩尔质量为$\frac{28g}{0.5mol}$=56g/mol,令烯烃的组成为(CH2)n,故14n=56,解得n=4,故该烯烃为C4H8,可能的结构为:CH2=CH-CH2CH3,CH3-CH=CH-CH3,CH2=C(CH3)2,
故答案为:CH2=CH-CH2CH3,CH3-CH=CH-CH3,CH2=C(CH3)2.
点评 本题以计算题形式考查有机物的推断、同分异构体等,难度中等,根据平均相对分子质量确定含有甲烷是解题的关键.

 全程金卷系列答案
全程金卷系列答案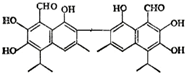 中央电视台曾报道纪联华超市在售的某品牌鸡蛋为“橡皮弹”,煮熟后蛋黄韧性胜过乒乓球,但经检测为真鸡蛋.专家介绍,这是由于鸡饲料里添加了棉籽饼,从而使鸡蛋里含有过多棉酚所致.其结构简式如图所示:下列说法不正确的是( )
中央电视台曾报道纪联华超市在售的某品牌鸡蛋为“橡皮弹”,煮熟后蛋黄韧性胜过乒乓球,但经检测为真鸡蛋.专家介绍,这是由于鸡饲料里添加了棉籽饼,从而使鸡蛋里含有过多棉酚所致.其结构简式如图所示:下列说法不正确的是( )| A. | 该化合物的分子式为:C30H30O8 | |
| B. | 1mol棉酚最多可与10mol H2加成,与6molNaOH反应 | |
| C. | 在一定条件下,可与乙酸反应生成酯类物质 | |
| D. | 该物质可以使酸性高锰酸钾溶液褪色 |
| A. | CH3CH2CH2CH3和CH3CH(CH3)2 | B. | CH2═C(CH3)2和CH3CH═CHCH3 | ||
| C. | CH3CH2OH和CH3OCH3 | D. | CH3CH2CH2COOH和CH3COOCH2CH3 |
| A. | 直线形;三角锥形 | B. | V形;三角锥形 | ||
| C. | 直线形;平面三角形 | D. | V形;平面三角形 |
| A. | ① | B. | ② | C. | ③ | D. | ④ |
| 元素代号 | A | B | D | E | G | H | I | J |
| 化合价 | -1 | -2 | +4、-4 | -1 | +5、-3 | +3 | +2 | +1 |
| 原子半径/nm | 0.071 | 0.074 | 0.077 | 0.099 | 0.110 | 0.143 | 0.160 | 0.186 |
| A. | A的单质能将E单质从HE的溶液中置换出来 | |
| B. | A、H、J的离子半径由大到小顺序是A>J>H | |
| C. | G元素的单质不存在同素异形体 | |
| D. | I在DB2中燃烧生成两种化合物 |


 (立方烷)
(立方烷)