题目内容
(2010?金华模拟)有如下化学反应:x1NaClO+y1Na2S5+z1NaOH-x2Na2SO4+y2NaCl+z2H2O,则下列判断正确的是( )
分析:可以根据氧化还原反应中得失电子守恒以及原子守恒来计算、推断.
解答:解:根据元素化合价的变化和电子守恒知识,可以知道氯元素化合价共降低2价,5个S的化合价共升高32价,根据最小公倍数是32,所以次氯酸钠的系数是16,氯化钠的系数是16,根据硫元素守恒,所以硫酸钠的前面是5,根据钠元素守恒则氢氧化钠的系数是8,结合氢元素守恒,水前面的系数是4,即16NaClO+Na2S5+8NaOH=5Na2SO4+16NaCl+4H2O.
A、根据配平后的反应可以知道x1=16,故A错误;
B、根据配平后的反应可以知道x1≠z1,故B错误;
C、根据配平后的反应可以知道x1+y1+z1=25,为奇数,故C错误;
D、根据配平后的反应可以知道y1+z1=24,故D正确.
故选D.
A、根据配平后的反应可以知道x1=16,故A错误;
B、根据配平后的反应可以知道x1≠z1,故B错误;
C、根据配平后的反应可以知道x1+y1+z1=25,为奇数,故C错误;
D、根据配平后的反应可以知道y1+z1=24,故D正确.
故选D.
点评:本题考查学生电子守恒法配平氧化还原反应方程式的方法,可以根据教材知识来回答,难度不大.

练习册系列答案
 学而优衔接教材南京大学出版社系列答案
学而优衔接教材南京大学出版社系列答案
相关题目
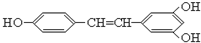 (2010?金华模拟)白藜芦醇广泛存在于食物(例如桑椹、花生、尤其是葡萄)中,它可能具有抗癌性.能够跟1摩尔该化合物起反应的Br2或H2的最大用量分别是( )
(2010?金华模拟)白藜芦醇广泛存在于食物(例如桑椹、花生、尤其是葡萄)中,它可能具有抗癌性.能够跟1摩尔该化合物起反应的Br2或H2的最大用量分别是( )