题目内容
【题目】下述转化关系可用于合成解痉药奥昔布宁的前体(化合物丙)。下列说法正确的是
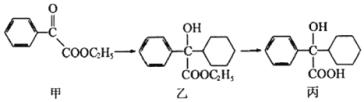
A. 化合物甲中的含氧官能团有羰基和酯基
B. 化合物乙与NaOH水溶液在加热条件下反应可生成化合物丙
C. 化合物乙不能发生消去反应
D. 化合物丙能和FeCl3溶液发生显色反应
【答案】A
【解析】
A.根据官能团的结构判断;B.化合物乙与NaOH水溶液在加热条件下反应可生成-COONa;C.-OH邻位C原子上有H原子,可发生消去反应生成C=C;D.化合物丙中不含酚羟基。
A.根据图示可知,化合物甲中的含氧官能团有羰基和酯基,选项A正确;B.乙与氢氧化钠水溶液反应生成的是羧酸盐和乙醇,无法达到化合物丙,选项B错误;C.化合物乙中,与羟基相邻的右侧C原子上含有H原子,能够发生消去反应,选项C错误;D.化合物丙分子中含有的是醇羟基,不能发生显色反应,选项D错误;答案选A。

 阅读快车系列答案
阅读快车系列答案【题目】研究+6价铬盐不同条件下微粒存在形式及氧化性,某小组同学进行如下实验:
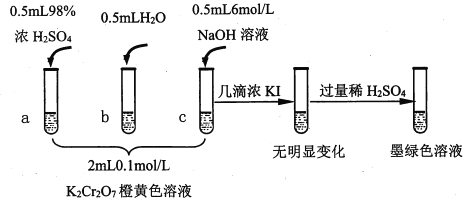
已知:Cr2O72- (橙色)+H2O![]() 2CrO42-(黄色)+2H+ △H= +13.8 kJ/mol,+6价铬盐在一定条件下可被还原为Cr3+,Cr3+在水溶液中为绿色。
2CrO42-(黄色)+2H+ △H= +13.8 kJ/mol,+6价铬盐在一定条件下可被还原为Cr3+,Cr3+在水溶液中为绿色。
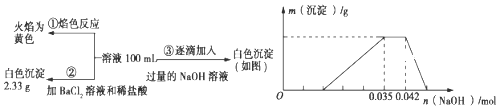
(1)试管c和b对比,推测试管c的现象是________。
(2)试管a和b对比,a中溶液橙色加深。甲认为温度也会影响平衡的移动,橙色加深不一定是c(H+)增大影响的结果;乙认为橙色加深一定是c(H+)增大对平衡的影响。你认为是否需要再设计实验证明?____(“是”或“否”),理由是_________________________________。
(3)对比试管a、b、c的实验现象,得到的结论是________________。
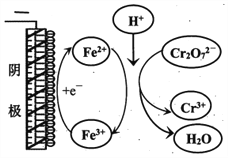
(4)试管c继续滴加KI溶液、过量稀H2SO4,分析上图的实验现象,得出的结论是_______;写出此过程中氧化还原反应的离子方程式________________。
(5)小组同学用电解法处理含Cr2O72-废水,探究不同因素对含Cr2O72-废水处理的影响,结果如下表所示(Cr2O72-的起始浓度,体积、电压、电解时间均相同)。
实验 | ⅰ | ⅱ | ⅲ | ⅳ |
是否加入Fe2(SO4)3 | 否 | 否 | 加入5g | 否 |
是否加入H2SO4 | 否 | 加入1mL | 加入1mL | 加入1mL |
电极材料 | 阴、阳极均为石墨 | 阴、阳极均为石墨 | 阴、阳极均为石墨 | 阴极为石墨,阳极为铁 |
Cr2O72-的去除率/% | 0.922 | 12.7 | 20.8 | 57.3 |
①实验ⅱ中Cr2O72-放电的电极反应式是________________。
②实验ⅲ