题目内容
【题目】如图是某课外小组制取乙炔并测定乙炔的某些性质的实验.

(1)写出实验室制取乙炔的化学方程式: ______.
(2)实验室制取乙炔时,分液漏斗中的液体 a通常是 ______.
(3)B溶液的作用是 ______.
(4)装置D中的现象是: ______.
(5)乙炔能否使溴的的四氯化碳溶液褪色?______(“能”或“不能”),若能写出完全反应原理_______________
(6)工业上常用乙炔、氯化氢等物质作原料来合成聚氯乙烯,请写出相关方程式 _______________
【答案】CaC2+2H2O→C2H2↑+Ca(OH)2 饱和食盐水 吸收杂质气体硫化氢 高锰酸钾溶液褪色 HC≡CH+2Br2→BrCH(Br)-(Br)CHBr CH≡CH+HCl![]() CH2=CHCl
CH2=CHCl 
【解析】
(1)实验室利用电石与水反应制取乙炔;
(2)电石与水反应速率太快,通常利用饱和食盐水代替水以减慢化学反应速率;
(3)此反应中会产生杂质气体硫化氢,会对乙炔性质实验造成干扰,据此解答;
(4)乙炔含有碳碳三键,能与高锰酸钾溶液反应使其褪色;
(5)溴水与乙炔发生加成反应;
(6)聚氯乙烯的单体是氯乙烯,乙炔与氯化氢发生加成生成氯乙烯,氯乙烯发生加聚生成聚氯乙烯,据此写出反应的方程式。
(1)电石与水反应生成乙炔和氢氧化钙,化学反应方程式为: CaC2+2H2O→C2H2↑+Ca(OH)2;
答案是: CaC2+2H2O→C2H2↑+Ca(OH)2;
(2)电石与水反应速率太快,通常利用饱和食盐水代替水以减慢化学反应速率;
答案是:饱和食盐水;
(3)此反应中会产生杂质气体硫化氢,会对乙炔性质实验造成干扰,利用硫酸铜溶液吸收硫化氢气体,以避免干扰后面乙炔性质的检验;
答案是:吸收杂质气体硫化氢;
(4)乙炔含有碳碳三键,能与高锰酸钾溶液反应,使高锰酸钾溶液褪色;
答案是:高锰酸钾溶液褪色;
(5)溴水与乙炔发生加成反应,反应方程式为: HC≡CH+2Br2→BrCH(Br)-(Br)CHBr;
答案是: HC≡CH+2Br2→BrCH(Br)-(Br)CHBr;
(6)聚氯乙烯的单体是氯乙烯,因此乙炔与氯化氢(1:1)反应生成氯乙烯,然后氯乙烯发生加聚生成聚氯乙烯,反应的方程式为:CH≡CH+HCl![]() CH2=CHCl;
CH2=CHCl; ;
;
故答案是:CH≡CH+HCl![]() CH2=CHCl;
CH2=CHCl;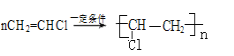 。
。





