题目内容
下表是某兴趣小组通过实验获得的稀硫酸与某金属反应的实验数据:
分析上述数据,回答下列问题:
(1)上述反应中,反应物的总能量比生成物的总能量 (选填“高”、“低”或“相等”)。
(2)实验1、2可得出的结论是 ;
实验3、4可得出的结论是 。
(3)若将该金属与铁用导线连接,插入盛有稀硫酸的烧杯中制作成原电池,观察到铁的表面有大量气泡。该金属的金属活动性比铁 (选填“强”或“弱”),铁电极上发生的电极反应式为 。
| 实验序号 | 金属 质量/g | 金属 状态 | c(H2SO4) mol/L | V(H2SO4) mL | 溶液温度/℃ | 金属消失的时间/s | |
| 反应前 | 反应后 | ||||||
| 1 | 0.10 | 丝 | 0.7 | 50 | 20 | 36 | 250 |
| 2 | 0.10 | 丝 | 0.8 | 50 | 20 | 35 | 200 |
| 3 | 0.10 | 丝 | 1.0 | 50 | 20 | 35 | 125 |
| 4 | 0.10 | 丝 | 1.0 | 50 | 35 | 50 | 50 |
(1)上述反应中,反应物的总能量比生成物的总能量 (选填“高”、“低”或“相等”)。
(2)实验1、2可得出的结论是 ;
实验3、4可得出的结论是 。
(3)若将该金属与铁用导线连接,插入盛有稀硫酸的烧杯中制作成原电池,观察到铁的表面有大量气泡。该金属的金属活动性比铁 (选填“强”或“弱”),铁电极上发生的电极反应式为 。
(12分)
(1)高(2分);
(2)反应物浓度越大,反应速率越快(3分)
反应温度越高,反应速率越快(3分)
(3)强(2分) 2H++2e-=H2↑ (2分)
(1)高(2分);
(2)反应物浓度越大,反应速率越快(3分)
反应温度越高,反应速率越快(3分)
(3)强(2分) 2H++2e-=H2↑ (2分)
略

练习册系列答案
相关题目
 2B(g) DH>0,在温度为T1、T2时,平衡体系中B的体积分数随压强变化的曲线如图所示。回答下列各题。
2B(g) DH>0,在温度为T1、T2时,平衡体系中B的体积分数随压强变化的曲线如图所示。回答下列各题。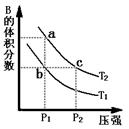
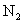 和3 mol
和3 mol 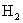 ,在一定条件下反应2min后,则得
,在一定条件下反应2min后,则得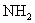 ,总质量为13.6g,如用
,总质量为13.6g,如用 气体通过灼热的装有催化剂(V2O5)的硬质玻璃管,反应后测得气体体积增大了b L(气体体积均在同温同压下测定),则下列叙述正确的是 ( )
气体通过灼热的装有催化剂(V2O5)的硬质玻璃管,反应后测得气体体积增大了b L(气体体积均在同温同压下测定),则下列叙述正确的是 ( )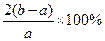
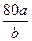

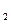 的体积分数为
的体积分数为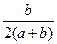
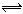 2C(g),2分钟后,B由2mol减少到1.2mol,则用单位内A的浓度变化表示的反应速率(VA)是 ( )
2C(g),2分钟后,B由2mol减少到1.2mol,则用单位内A的浓度变化表示的反应速率(VA)是 ( )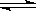 2SO3,经5S后,SO3的浓度增加了0.4mol/L,在这段时间内用O2表示的反应速率为多少?
2SO3,经5S后,SO3的浓度增加了0.4mol/L,在这段时间内用O2表示的反应速率为多少? CO(g) + H2(g) 在一可变容积的密闭容器中进行,下列条件的改变能使瞬间正反应速率增大的是
CO(g) + H2(g) 在一可变容积的密闭容器中进行,下列条件的改变能使瞬间正反应速率增大的是