题目内容
Ⅰ.盖斯定律在生产和科学研究中有很重要的意义。有些反应的反应热虽然无法直接测得,但可通过间接的方法测定。现根据下列的5个反应(由氨气、HCl和水制备NH4C1水溶液)。请判断反应④的反应热:ΔH= 。
① NH3(g) + HCl(g) = NH4Cl(s) ΔH=-176kJ·mol–1
② NH3(g) + H2O(l) = NH3(aq) ΔH=-35.1 kJ·mol–1
③ HCl(g) + H2O(l) = H Cl(aq) ΔH=-72.3 kJ·mol–1
Cl(aq) ΔH=-72.3 kJ·mol–1
④ NH4C1(s) + H2O(1) = NH4C1(aq)
⑤ NH3(aq) + HCl(aq) = NH4C1(aq) ΔH= -52.3 kJ·mol–1
HCl(aq) = NH4C1(aq) ΔH= -52.3 kJ·mol–1
Ⅱ.N2O5是一种新型硝化剂,其性质和制备受到人们的关注。现以H2、O2、熔融盐Na2CO3组成的燃料电池,采用电解法制备N2O5,装置如图所示,其中Y为CO2。
写出石墨I电极上发生反应的电极反应式 。
在电解池中生成N2O3的电极反应式为 。
Ⅲ.烟气的脱硫(除SO2)技术和脱硝(除NOx)技术都是环境科学研究的热点。
⑴烟气脱硫、脱硝的环境意义是 。
(2)目前,科学家正在研究一种以乙烯作为还原剂的脱硝(NO)原理,其脱硝机理示意图如下图1,脱硝率与温度、负载率(分子筛中催化剂的质量分数)的关系如图2所示。
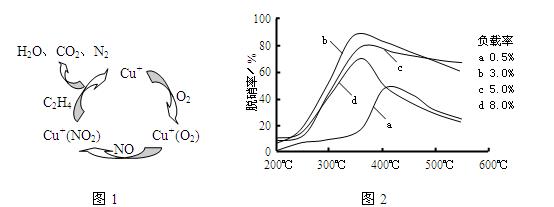
①写出该脱硝原理总反应的化学方程式: 。②为达到最佳脱硝效果,应采取的条件是 。
① NH3(g) + HCl(g) = NH4Cl(s) ΔH=-176kJ·mol–1
② NH3(g) + H2O(l) = NH3(aq) ΔH=-35.1 kJ·mol–1
③ HCl(g) + H2O(l) = H
 Cl(aq) ΔH=-72.3 kJ·mol–1
Cl(aq) ΔH=-72.3 kJ·mol–1④ NH4C1(s) + H2O(1) = NH4C1(aq)
⑤ NH3(aq) +
 HCl(aq) = NH4C1(aq) ΔH= -52.3 kJ·mol–1
HCl(aq) = NH4C1(aq) ΔH= -52.3 kJ·mol–1Ⅱ.N2O5是一种新型硝化剂,其性质和制备受到人们的关注。现以H2、O2、熔融盐Na2CO3组成的燃料电池,采用电解法制备N2O5,装置如图所示,其中Y为CO2。

写出石墨I电极上发生反应的电极反应式 。
在电解池中生成N2O3的电极反应式为 。
Ⅲ.烟气的脱硫(除SO2)技术和脱硝(除NOx)技术都是环境科学研究的热点。
⑴烟气脱硫、脱硝的环境意义是 。
(2)目前,科学家正在研究一种以乙烯作为还原剂的脱硝(NO)原理,其脱硝机理示意图如下图1,脱硝率与温度、负载率(分子筛中催化剂的质量分数)的关系如图2所示。

①写出该脱硝原理总反应的化学方程式: 。②为达到最佳脱硝效果,应采取的条件是 。
Ⅰ、ΔH=+16.3 kJ·mol–1;
Ⅱ、(3)H2+CO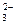 -2e-=CO2+H2O;阳极:N2O4+2HNO3-2e-=2N2O5+2H+;
-2e-=CO2+H2O;阳极:N2O4+2HNO3-2e-=2N2O5+2H+;
Ⅲ、⑴防止酸雨的发生,⑵6NO+3O2+2C2H4 3N2+4CO2+4H2O(其他合理配平方式也对);②350℃、负载率3%。
3N2+4CO2+4H2O(其他合理配平方式也对);②350℃、负载率3%。
Ⅱ、(3)H2+CO
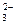 -2e-=CO2+H2O;阳极:N2O4+2HNO3-2e-=2N2O5+2H+;
-2e-=CO2+H2O;阳极:N2O4+2HNO3-2e-=2N2O5+2H+;Ⅲ、⑴防止酸雨的发生,⑵6NO+3O2+2C2H4
 3N2+4CO2+4H2O(其他合理配平方式也对);②350℃、负载率3%。
3N2+4CO2+4H2O(其他合理配平方式也对);②350℃、负载率3%。略

练习册系列答案
 走进文言文系列答案
走进文言文系列答案
相关题目

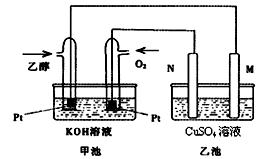
 下),理论上需通入乙醇 g?
下),理论上需通入乙醇 g? 2NH3(g);△H=-92.4kJ·mol-1
2NH3(g);△H=-92.4kJ·mol-1 C(g) +D(g)过程中的能量变化如图所示,则下列说法正确的是
C(g) +D(g)过程中的能量变化如图所示,则下列说法正确的是