题目内容
14.下列叙述中,正确的是( )| A. | Cl2能与金属活动顺序表中大多数金属反应 | |
| B. | 待测溶液中加入氯化钡溶液有白色沉淀生成,再加稀硝酸,沉淀不消失,一定有硫酸根离子 | |
| C. | 在用AgNO3溶液检验Cl-时,一般先在被检测的溶液中滴入少量的稀硝酸使其酸化,以排除干扰离子 | |
| D. | 硅是应用广泛的半导体材料,常温下化学性质不活泼,是光导纤维的主要成分 |
分析 A.氯气具有强氧化性,为活泼非金属性单质;
B.AgCl为不溶于水、不溶于酸的白色沉淀;
C.氯离子的检验借助氯化银为不溶于硝酸的白色沉淀,注意排除碳酸根离子等杂质离子的干扰;
D.光导纤维的主要成分是二氧化硅.
解答 解:A.氯气具有强氧化性,可与大多数金属反应,故A正确;
B.因AgCl为不溶于水、不溶于酸的白色沉淀,则待测液中加入氯化钡溶液有白色沉淀生成,再加稀盐酸,沉淀不消失,则待测液中含有的可能是硫酸根离子或银离子,故B错误;
C.氯离子的检验借助氯化银为不溶于硝酸的白色沉淀,一般先在被检测的溶液中滴入少量的稀硝酸使其酸化,以排除干扰离子,故C正确;
D.光导纤维的主要成分是二氧化硅,不是硅,故D错误;
故选:AC.
点评 本题考查了离子的检验、氯气、二氧化硅的性质,题目难度不大,熟悉相关物质的性质是解题关键.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
19.一定温度下,对于反应N2+O2?2NO在密闭容器中进行,下列措施能增大反应速率的是( )
| A. | 缩小体积使压强增大 | B. | 恒容,充入N2 | ||
| C. | 恒容充入氦气 | D. | 恒压充入氦气 |
19.X+的结构示意图为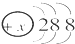 ,则X元素在元素周期表中位于( )
,则X元素在元素周期表中位于( )
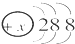 ,则X元素在元素周期表中位于( )
,则X元素在元素周期表中位于( )| A. | 第三周期0族 | B. | 第四周期第ⅠA族 | C. | 第三周期第ⅠA族 | D. | 第三周期第ⅦA族 |
3. 用如图所示装置进行下列实验,实验结果与预测现象不一致的是( )
用如图所示装置进行下列实验,实验结果与预测现象不一致的是( )
 用如图所示装置进行下列实验,实验结果与预测现象不一致的是( )
用如图所示装置进行下列实验,实验结果与预测现象不一致的是( )| 选项 | ①中物质 | ②中物质 | 预测①中现象 |
| A | 酚酞溶液 | 浓氨水 | 无色变红色 |
| B | 湿润红布条 | 饱和氯水 | 红布条褪色 |
| C | 淀粉KI溶液 | 浓硝酸 | 无明显变化 |
| D | 硝酸银溶液 | 浓盐酸 | 有白色沉淀 |
| A. | A | B. | B | C. | C | D. | D |
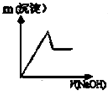
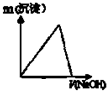

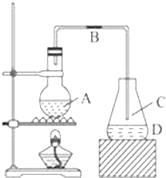 某化学课外小组用如图装置制取溴苯,请按要求完成下列小题:
某化学课外小组用如图装置制取溴苯,请按要求完成下列小题: .
.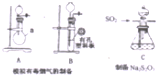 某化工厂排放了大量有毒气体,其主要成分是SO2、CO2、N2和O2,某研究性学习小组在实验室利用右图装置制备模拟有毒烟气,同时利用模拟有毒烟气中的SO2制取硫代硫酸钠晶体(Na2S2O3•5H2O),并进一步实验测定该晶体的纯度.查阅资料得知:①将SO2通入按一定比例配制成的Na2S和Na2CO3的混合溶液中,可制得Na2S2O3•5H2O;②KI3溶液为碘单质的碘化钾溶液;③硫代硫酸钠(Na2S2O3)具有较强的还原性,回答下列问题:
某化工厂排放了大量有毒气体,其主要成分是SO2、CO2、N2和O2,某研究性学习小组在实验室利用右图装置制备模拟有毒烟气,同时利用模拟有毒烟气中的SO2制取硫代硫酸钠晶体(Na2S2O3•5H2O),并进一步实验测定该晶体的纯度.查阅资料得知:①将SO2通入按一定比例配制成的Na2S和Na2CO3的混合溶液中,可制得Na2S2O3•5H2O;②KI3溶液为碘单质的碘化钾溶液;③硫代硫酸钠(Na2S2O3)具有较强的还原性,回答下列问题: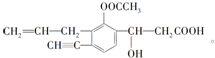
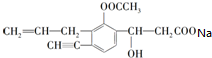 +CO2↑+H2O.
+CO2↑+H2O.