题目内容
15.美国《科学》杂志评出2001年十大科技成就,名列榜首的是纳米电子学,其中美国一家公司制造的第一批纳米碳管晶体管,发明了种用电子的波性来仁慈信息的“导线”已知纳米材料是指微粒直径在1-100nm的材料.下列叙述正确的是( )| A. | 纳米碳管是一种新型的高分子化合物 | |
| B. | 纳米碳管的化学性质稳定 | |
| C. | 纳米碳管的结构和性质与金刚石相同 | |
| D. | 纳米碳管导电属于化学变化 |
分析 A.纳米碳管只含一种元素;
B.碳单质在常温下的化学性质稳定;
C.碳纳米管是管状结构,金刚石是立体网状结构;
D.纳米碳管导电的过程中没有新物质生成.
解答 解:A.碳纳米管是由碳原子组成的单质,只有一种元素,不属于化合物,故A错误;
B.碳单质在常温下的化学性质稳定,所以纳米碳管的化学性质稳定,故B正确;
C.碳纳米管是管状结构,金刚石是立体网状结构,两者结构不同;由于碳原子的排列方式不同,性质也不完全相同,故C错误;
D.纳米碳管导电的过程中没有新物质生成,属于物理变化,故D错误;
故选B.
点评 本题主要考查纳米材料,考查学生获取信息,筛选信息结合已有知识分析、解决问题的能力,题目难度不大.

练习册系列答案
相关题目
6. 硫酸的年产量高低常用于衡量一个国家化工生产水平的高低.
硫酸的年产量高低常用于衡量一个国家化工生产水平的高低.
(1)以黄铁矿为原料生产SO2时反应的化学方程式为:4FeS2 +11 O2$\frac{\underline{\;高温\;}}{\;}$2Fe2O3+8SO2,该反应在沸腾炉中进行(填设备名称);
(2)某科研小组测得某硫酸工厂生产工厂中SO2的平衡转化率与外部条件的关系如下表所示,则生产过程中,最适合的生产条件是1个大气压、400℃;
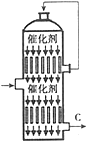
(3)接触室内有一热交换器,其作用是预热原料气,吸收反应放出的热量,若将从C处(如图)出来的气体通入BaCl2溶液中,则主要负电离子方程式为(写总反应式)SO3+Ba2++H2O=BaSO4↓+2H+;
(4)下列做法中,与提高硫酸工业的经济效益无关的是d;
a.适当地对黄铁矿进行粉碎
b.在接触室中使用适当过量的O2
c.利用生产中的余热发电或供暖
d.对废水进行无害化处理后再排放
(5)硫酸工业会产生许多对环境有害的物质,因此无论是工厂厂址的选择还是生产过程中有害成分的处理都要充分考虑环保的要求;
①某市计划建一个硫酸工厂,厂址有A、B、C三个地方可供选择,假设最终该厂建在B地,你认为选择B地建厂的理由是(至少回答两点)B地远离硫酸的消耗中心、B地远离人品稠密的地方;
②将尾气中SO2在一定条件下转化为CaSO4,然后利用焦炭将其转化为CaS(另有一种可燃性气体生成)具有重要的意义,写出CaSO4转化为CaS的化学方程式CaSO4+4C$\frac{\underline{\;高温\;}}{\;}$CaS+4CO;
(6)若用等质量的硫磺,FeS2生产硫酸,假设原料的总利用率均为90%,则二者得到的硫酸质量比为15:8.
 硫酸的年产量高低常用于衡量一个国家化工生产水平的高低.
硫酸的年产量高低常用于衡量一个国家化工生产水平的高低.(1)以黄铁矿为原料生产SO2时反应的化学方程式为:4FeS2 +11 O2$\frac{\underline{\;高温\;}}{\;}$2Fe2O3+8SO2,该反应在沸腾炉中进行(填设备名称);
(2)某科研小组测得某硫酸工厂生产工厂中SO2的平衡转化率与外部条件的关系如下表所示,则生产过程中,最适合的生产条件是1个大气压、400℃;
| 压强 (Pa) 温度 (℃) | 1.013×105 | 5.065×105 | 10.13×105 | 15.195×105 |
| 400 | 99.61% | 99.72% | 99.84% | 99.88×105 |
| 500 | 96.75% | 97.67% | 98.52% | 98.94% |
| 600 | 85.20% | 88.97% | 92.76% | 94.68% |
(4)下列做法中,与提高硫酸工业的经济效益无关的是d;
a.适当地对黄铁矿进行粉碎
b.在接触室中使用适当过量的O2
c.利用生产中的余热发电或供暖
d.对废水进行无害化处理后再排放
(5)硫酸工业会产生许多对环境有害的物质,因此无论是工厂厂址的选择还是生产过程中有害成分的处理都要充分考虑环保的要求;
①某市计划建一个硫酸工厂,厂址有A、B、C三个地方可供选择,假设最终该厂建在B地,你认为选择B地建厂的理由是(至少回答两点)B地远离硫酸的消耗中心、B地远离人品稠密的地方;
②将尾气中SO2在一定条件下转化为CaSO4,然后利用焦炭将其转化为CaS(另有一种可燃性气体生成)具有重要的意义,写出CaSO4转化为CaS的化学方程式CaSO4+4C$\frac{\underline{\;高温\;}}{\;}$CaS+4CO;
(6)若用等质量的硫磺,FeS2生产硫酸,假设原料的总利用率均为90%,则二者得到的硫酸质量比为15:8.
3.下列说法正确的是( )
| A. | 组成元素相同且各元素质量分数也相同的一定互为同分异构体 | |
| B. | 相对分子质量相同的有机物一定为同分异构体 | |
| C. | 有相同的分子通式且分子组成上相差一个或若干个CH2原子团的物质一定互为同系物 | |
| D. | 结构不同,性质相似,化学式相同的物质互称同分异构体 |
10.下列各组混合物中,能用分液漏斗进行分离的是( )
| A. | 醋酸和水 | B. | 碘和苯 | C. | 水和溴苯 | D. | 汽油和煤油 |
7.如图是298K 时N2与H2反应过程中能量变化的曲线图.下列叙述不正确的是( )
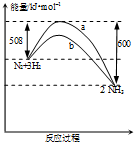

| A. | 加入催化剂,该化学反应的活化能和反应热都改变 | |
| B. | b曲线是加入催化剂时的能量变化曲线 | |
| C. | 该反应的热化学方程式为N2(g)+3H2(g)?2NH3(g);△H=-92kJ•mol-1 | |
| D. | 在温度、体积一定的条件下,通入lmol N2和3molH2 反应后放出的热量为Q1kJ,则Q1<92 |
4.下列溶液中各微粒的浓度关系正确的是( )
| A. | pH=4的盐酸中:c(H+)=4.0mol•L-1 | |
| B. | NH4Cl溶液中:c(Cl-)=c(NH4+) | |
| C. | NaCl溶液中:c(Na+)+c(H+)=c(Cl-)+c(OH-) | |
| D. | Na2CO3溶液中:c(HCO3-)+c(H2CO3)+c(CO32-)=2c(Na+) |
5.下列叙述正确的是( )
| A. | 乙醇能使酸性KMn04溶液和酸性K2Cr207溶液褪色,均被氧化成乙酸 | |
| B. | 向酸性高锰酸钾中加入草酸溶液,随着反应的进行,反应速率逐渐减小 | |
| C. | 向某溶液中滴加BaCl2溶液出现白色沉淀,加稀硝酸,沉淀不溶解,说明该溶液中存在S042-或S032- | |
| D. | 实验室提纯混有少量氯化钠的硝酸钾,通常采用重结晶的方法 |
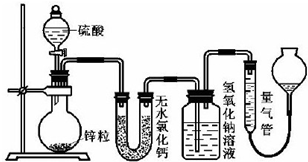
 ,该化合物中含有的化学键有离子键、共价键
,该化合物中含有的化学键有离子键、共价键