题目内容
【题目】海洋是一个巨大的化学资源宝库。 海水综合利用的部分流程如下:

已知:Br2的沸点为59℃,微溶于水,有毒性和强腐蚀性。
(1)电解饱和 NaCl 溶液的化学方程式为_____________________________________。粗盐中常含 Ca2+、Mg2+、SO42-等杂质离子,可依次加入NaOH、___________、___________、盐酸试剂来进行提纯。
(2)下列方法不可用于海水淡化的是________(填字母代号)。
A. 蒸馏法 B. 萃取法 C. 离子交换法 D. 电渗析法
(3)工业上用电解法制Mg 时,通常在MgCl2中加入适量 CaCl2,其原因是:①___________; ②增加电解质的密度,便于分离出熔融的镁。
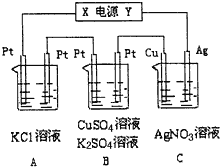
(4) 利用右图所示装置从母液中提取溴,在 B 瓶中得到较浓的溴水。实验方案为:关闭b、d,打开a、c,由a 向A中缓慢通入________至反应完全;关闭a、c,打开b、d、e,由b向A中鼓入足量__________, 同时由 e 向 B 中通入足量_________;关闭b、e,打开a,再由a 向B中缓缓鼓入足量___________ (实验中须使用的试剂有:SO2、Cl2、热空气) 。

【答案】 2NaCl + 2H2O ![]() Cl2↑ + H2↑ + 2NaOH BaCl2 Na2CO3 B 使 MgCl2 熔融温度降低, 从而减少能量消耗 Cl2 热空气 SO2 Cl2
Cl2↑ + H2↑ + 2NaOH BaCl2 Na2CO3 B 使 MgCl2 熔融温度降低, 从而减少能量消耗 Cl2 热空气 SO2 Cl2
【解析】(1)惰性电极电解NaCl溶液,阳极上是氯离子失电子,2Cl--2e-=Cl2↑,阴极上是氢离子得电子,2H++2e-=H2↑,由两极上的电极反应可以得到总反应为2Cl-+2H2O![]() H2↑+Cl2↑+2OH-,钙离子用碳酸根离子沉淀,除钙离子加入碳酸钠转化为沉淀,但是加入的碳酸钠要放在加入的氯化钡之后,这样碳酸钠会除去反应剩余的氯化钡,离子都沉淀了,再进行过滤,最后再加入盐酸除去反应剩余的氢氧根离子和碳酸根离子,则试剂可依次加入NaOH、BaCl2、Na2CO3、HCl;
H2↑+Cl2↑+2OH-,钙离子用碳酸根离子沉淀,除钙离子加入碳酸钠转化为沉淀,但是加入的碳酸钠要放在加入的氯化钡之后,这样碳酸钠会除去反应剩余的氯化钡,离子都沉淀了,再进行过滤,最后再加入盐酸除去反应剩余的氢氧根离子和碳酸根离子,则试剂可依次加入NaOH、BaCl2、Na2CO3、HCl;
(2)A.蒸馏法,是把水从水的混合物中分离出来,得到纯净的水,故A正确;B.萃取法,对于微溶于水的有机物,可用萃取法,水中没有微溶于水的有机物,故B错误;C.通过离子交换树脂可以除去海水中的离子,从而达到淡化海水的目的,故C正确;D.利用电渗析法可使相应的离子通过半透膜以达到硬水软化的效果,故D正确;故答案为B;
(3)离子浓度越大其熔融盐的导电性越强,在MgCl2中加入CaCl2,进行电解,增大离子浓度,从而增大熔融盐的导电性,使氯化镁熔融温度降低,从而减少冶炼过程中的能量消耗;
(4)A中海水用硫酸酸化,关闭a、c,打开b、d、e,由b向A中通入热空气和氯气,发生氧化还原反应生成溴,空气将溴吹出,同时由e向B中通入足量SO2,发生Br2+SO2+H2O═2HBr+H2SO4,富集后再关闭b、e,打开a,再由a向B中缓慢通入足量Cl2,生成Br2。