题目内容
(一)、将2 mol SO2和1 mol
O2气体在1L的容器中混合,在一定条件下发生如下反应:2SO2(g)+O2 (g) 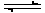 2SO3 (g)。若经过2s后测得SO3的浓度为0.6 mol/ L。试计算:(1)O2的化学反应速率V(O2)= ; (2)2s时的O2浓度 。
2SO3 (g)。若经过2s后测得SO3的浓度为0.6 mol/ L。试计算:(1)O2的化学反应速率V(O2)= ; (2)2s时的O2浓度 。
(二)、某温度时,在2 L的密闭容器中,X、Y、Z三种物质的量随时间的变化曲线如下图所示。
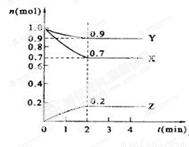
(1)X的转化率是
(2)由图中所给数据进行分析,该反应的化学方程式为 ;
(3)反应从开始至2分钟末,用Z的浓度变化表示的平均反应速率为v(Z)= ;
(4)当反应进行到第 min,该反应达到平衡。
(1) υ(O2)="0" .15mol/(L·s) c(O2)=0.7 mol/L
(2) 30% 3X+Y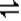 2Z
0.05mol/(l.·min) 2
2Z
0.05mol/(l.·min) 2
【解析】
试题分析:(一) 2s后测得SO3的浓度为0.6 mol/ L,所以V(O2)="0.5"
V(SO2)=0.5 0.6/2=0 .15mol/(L·s),2s时的O2浓度=1-0 .15
0.6/2=0 .15mol/(L·s),2s时的O2浓度=1-0 .15 2=0.7 mol/L;
2=0.7 mol/L;
(二)由图可以知道,每反应0.1molY,和0.3molX就生成了0.2mol的Z,所以其反应的化学方程式为3X+Y 2Z, X的转化率=0.3/1
2Z, X的转化率=0.3/1 100%=30%,(3)反应从开始至2分钟末,用Z的浓度变化表示的平均反应速率为v(Z)=0.2/2/2= 0.05mol/(l.·min);(4)由图可以看出,当反应时间为2min时,各物质的浓度均不再变化,所以当反应进行到第2min,该反应达到平衡。
100%=30%,(3)反应从开始至2分钟末,用Z的浓度变化表示的平均反应速率为v(Z)=0.2/2/2= 0.05mol/(l.·min);(4)由图可以看出,当反应时间为2min时,各物质的浓度均不再变化,所以当反应进行到第2min,该反应达到平衡。
考点:化学平衡,反应速率
点评:本题考查了化学平衡,反应速率的相关计算,是高考考查的重点,该题综合性强,但难度不大。

 开心蛙口算题卡系列答案
开心蛙口算题卡系列答案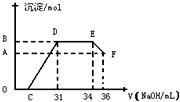 (2012?长宁区一模)Ⅰ将a mol的Na2O2和bmol NaHCO3固体混合后,在密闭容器中加热到250℃,让其充分反应,假设NaHCO3分解产生的CO2与Na2O2反应完后,H2O再与Na2O2反应.
(2012?长宁区一模)Ⅰ将a mol的Na2O2和bmol NaHCO3固体混合后,在密闭容器中加热到250℃,让其充分反应,假设NaHCO3分解产生的CO2与Na2O2反应完后,H2O再与Na2O2反应. CH3OH(g) ΔH1
CH3OH(g) ΔH1