题目内容
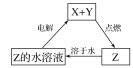
【题目】为除去粗盐中的Ca2+、Mg2+、SO42-以及泥沙等杂质,某同学设计了一种制备精盐的实验方案,步骤如下(用于沉淀的试剂稍过量):
称取粗盐![]()
![]()
![]()
![]()
![]() 滤液
滤液![]()
![]() 精盐
精盐
(1)如何检验该粗盐中含有SO42-___。
(2)第④步中加入过量的Na2CO3的目的是___。
(3)蒸发结晶需要的玻璃仪器___。
(4)若先加适量盐酸再过滤,将对实验结果产生影响,其原因是______。(用离子方程式结合文字解释)
【答案】取少量待测液于试管中,先加入过量稀盐酸酸化,再加入几滴氯化钡溶液,有白色沉淀,说明待测液中含有硫酸根离子 完全去除钙离子和钡离子 玻璃棒、蒸发皿、酒精灯 盐酸会将前面生成的沉淀溶解,CaCO3+2H+=CO2↑+H2O+Ca2+、BaCO3+2H+=CO2↑+H2O+Ba2+、Mg(OH)2+2H+=Mg2++ 2H2O
【解析】
为除去粗盐中的Ca2+、Mg2+、SO42-以及泥沙等杂质,根据流程图,将粗盐溶于水配成溶液,加入氯化钡溶液沉淀硫酸根离子,加入NaOH沉淀镁离子,再加入碳酸钠沉淀钙离子和钡离子,过滤后,加入适量盐酸除去过量的氢氧化钠和碳酸钠,最后蒸发结晶烘干得到精盐,据此分析解答。
(1)检验该粗盐中含有SO42-,可以取少量待测液于试管中,先加入过量稀盐酸酸化,再加入几滴氯化钡溶液,有白色沉淀,说明待测液中含有硫酸根离子,故答案为:取少量待测液于试管中,先加入过量稀盐酸酸化,再加入几滴氯化钡溶液,有白色沉淀,说明待测液中含有硫酸根离子;
(2)碳酸钠可以将钙离子以及过量的钡离子沉淀下来,反应原理是Ca2++CO32-=CaCO3↓、Ba2++CO32-=BaCO3↓,故答案为:完全去除钙离子和钡离子;
(3)蒸发结晶需要的玻璃仪器有玻璃棒、蒸发皿、酒精灯,故答案为:玻璃棒、蒸发皿、酒精灯;
(4)若先用盐酸调pH再过滤,氢氧化镁沉淀、碳酸钙沉淀和碳酸钡沉淀均会和盐酸反应,将对实验结果产生影响,反应的离子方程式分别为CaCO3+2H+=CO2↑+H2O+Ca2+、BaCO3+2H+=CO2↑+H2O+Ba2+、Mg(OH)2+2H+=Mg2++2H2O,因此需要先过滤,再加入适量盐酸,故答案为:盐酸会将前面生成的沉淀溶解,CaCO3+2H+=CO2↑+H2O+Ca2+、BaCO3+2H+=CO2↑+H2O+Ba2+、Mg(OH)2+2H+=Mg2++2H2O。

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案【题目】中国传统文化对人类文明贡献巨大,古代文献中记载了古代化学研究成果。下列常见古诗文对应的化学知识正确的是
常见古诗文记载 | 化学知识 | |
A | 《梦溪笔谈》中对宝剑的记载:“古人以剂钢为刃,柔铁为茎干,不尔则多断折” | 铁的合金硬度比纯铁的大,熔点比纯铁的高 |
B | 《本草纲目拾遗》中对强水的记载:“性最烈,能蚀五金,其水甚强,惟玻璃可盛” | 强水为氢氟酸 |
C | 《天工开物》中记载:凡火药,硫为纯阳,硝为纯阴 | 硫指的是硫黄.硝指的是硝酸钾 |
D | 《泉州府志》中记载:安南人黄姓者为宅煮糖,墙塌压糖,去土而糖白,后人遂效之 | 糖白的过程发生了化学变化 |
A. AB. BC. CD. D