题目内容
分子式为C4H9Br的有机物的可能结构有
| A.2种 | B.3种 | C.4种 | D.5种 |
C
专题:同分异构体的类型及其判定.
分析:化学上,同分异构体是一种有相同化学式,有同样的化学键而有不同的原子排列的化合物.简单地说,化合物具有相同分子式,但具有不同结构的现象,叫做同分异构现象;具有相同分子式而结构不同的化合物互为同分异构体.
解答:分子式为C4H9Br从饱和度看只能是饱和溴代烷烃,同分异构只是溴在碳上面链接位置不同而已,因为丁烷有两种同分异构体,它们一溴代物的种数即为C4H9Br的种数,正丁烷两种一溴代物,异丁烷两种一溴代物,共4种,所以分子式为C4H9Br的同分异构体共有4种.故选C.
点评:本题考查学生同分异构体的概念和应用知识,可以根据所学知识来回答,难度不大.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
 =”),基态C原子的电子排布式为 。
=”),基态C原子的电子排布式为 。
 H、
H、 H和
H和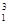 H互为同位素
H互为同位素 互为同系物
互为同系物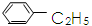 互 C2H5和
互 C2H5和 互为同分异构体
互为同分异构体