题目内容
【题目】向一定量的NaOH溶液中逐滴加入AlCl3溶液,生成沉淀Al(OH)3的量随AlCl3加入量的变化关系如图所示。则下列离子组在对应的溶液中一定能大量共存的是
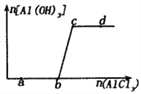
A. a点对应的溶液中: Na+、K+、SO42-、HCO3-
B. b点对应的溶液中:Na+、ClO-、SO42-、Cl-
C. c点对应的溶液中: Ag+、H+、Ca2+、NO3-
D. d 点对应的溶液中: K+、NH4+、OH-、Cl-
【答案】B
【解析】A.a点溶液显碱性,NaOH过量,则不可能存在HCO3-,不能共存,A错误;B.b点恰好生成偏铝酸钠,溶液显碱性,Na+、ClO-、SO42-、Cl-不反应,能大量存在,B正确;C.c点偏铝酸钠与氯化铝恰好完全反应生成氢氧化铝,还生成氯化钠,则不可能存在Ag+,不能共存,C错误;D.d点为氯化铝溶液,氢氧根与铵根以及铝离子反应,不能大量共存,D错误,答案选B。

练习册系列答案
相关题目
【题目】表为元素周期表的一部分:
IA | IIA | IIIA | IVA | VA | VIA | VIIA | ||
二 | C | N | ① | |||||
三 | ② | ③ | ④ | P | ⑤ | ⑥ |
请填写下列空白:
(1)表中元素,原子半径最大的是(填写元素符号);①的核外电子排布式;③和⑥两元素形成化合物的电子式为 .
(2)②③④三种元素最高价氧化物对应的水化物中,碱性最强的是(填化学式).
(3)比较④、⑤两种元素的简单离子半径:>(填离子符号);元素④最高价氧化物对应的水化物与硝酸反应的离子方程式为 .
(4)列举一个事实来证明元素①比元素⑤的非金属性强 .
(5)若8g甲烷气体完全燃烧生成液态水时放出445.15kJ的热量,请写出其热化学方程式 .